 Suite de l’examen des éléments mis en avant dans Le Point par Jacques Balthazart à l’appui de la théorie de la « différenciation sexuelle » du comportement humain qu’il promeut. Dans cette seconde partie, il sera question de son invocation de l’existence chez l’humain d’une « bonne dizaine de noyaux sexuellement différenciés » visibles uniquement post-mortem sur des coupes histologiques. Ce sujet mérite qu’on s’y penche en détail, car des données soigneusement choisies et présentées de manière fallacieuse concernant certains de ces noyaux sont au cœur du discours de Jacques Balthazart.
Suite de l’examen des éléments mis en avant dans Le Point par Jacques Balthazart à l’appui de la théorie de la « différenciation sexuelle » du comportement humain qu’il promeut. Dans cette seconde partie, il sera question de son invocation de l’existence chez l’humain d’une « bonne dizaine de noyaux sexuellement différenciés » visibles uniquement post-mortem sur des coupes histologiques. Ce sujet mérite qu’on s’y penche en détail, car des données soigneusement choisies et présentées de manière fallacieuse concernant certains de ces noyaux sont au cœur du discours de Jacques Balthazart.
___________________________
PLAN
I à IV : voir la partie 1
V. Des noyaux plus gros tantôt « chez l’homme », tantôt « chez la femme », différenciés comme « chez l’animal » par la testostérone périnatale
– De la sexuation de certains noyaux et comportements des oiseaux chanteurs
– Le noyau INAH-1 de l’hypothalamus
– Le noyau INAH-2 de l’hypothalamus
– Le noyau INAH-3 de l’hypothalamus
– Le noyau INAH-4 de l’hypothalamus
– Le noyau supraoptique de l’hypothalamus (SON)
– Le noyau du lit de la strie terminale (BST ou BNST)
– Le noyau suprachiasmatique de l’hypothalamus (SCN)
– Le noyau paraventriculaire de l’hypothalamus (PVN)
– Le noyau ventromédian de l’hypothalamus (VMN ou VMH)
– Le noyau arqué ou infundibulaire de l’hypothalamus (INF ou arcuate nucleus)
– Les corps mamillaires de l’hypothalamus
– Synthèse
Chapitres VI et suivants : à suivre (partie 3)
____________________________
V. Des noyaux plus gros tantôt « chez l’homme », tantôt « chez la femme », différenciés comme « chez l’animal » par la testostérone périnatale
Dans deux passages de l’interview, Jacques Balthazart invoque des données concernant des petits amas ou groupes relativement denses de neurones qui n’ont à ce jour été étudiés que sur des coupes histologiques de cerveaux de personnes décédées, les outils non invasifs d’imagerie in vivo n’étant pas encore assez performants.
§1 : « À la Renaissance […] on a au contraire constaté qu’il n’y avait pas de différences flagrantes d’un point de vue anatomique entre les cerveaux des femmes et des hommes. […] Mais en 1976, Fernando Nottebohm […] allait injecter de la testostérone à des canaris femelles, qui vont se mettre à chanter comme les mâles. C’est là qu’on découvre que les noyaux […] contrôlant le chant sont plus volumineux chez le mâle que chez la femelle, de deux à trois fois plus chez le canari à cinq fois plus chez le diamant mandarin. […] Roger Gorski, de l’UCLA, a découvert chez le rat un autre noyau dans l’aire préoptique également cinq fois plus volumineux chez le mâle que chez la femelle. Les recherches se sont emballées et étendues dans bien des espèces : cochons d’Inde, moutons, singes… Et chez les humains ? L’espèce humaine n’est en rien exceptionnelle. Dans les années 1980, Dick Swaab, à Amsterdam, a le premier trouvé un groupe de neurones différenciés selon le sexe. Les études sur cerveaux humains sont évidemment plus compliquées, car ces noyaux sexuellement différenciés sont des structures très petites qu’on ne peut voir que sur des coupes histologiques, et donc avec des donneurs morts. Mais une bonne dizaine de noyaux sexuellement différenciés ont ainsi été repérés dans le système nerveux central humain. Ils sont parfois plus volumineux chez l’homme, parfois plus chez la femme. »
§2 : «le gène SRY présent sur le chromosome Y va aboutir à la formation de deux testicules qui secréteront de la testostérone pendant une partie bien spécifique de la vie embryonnaire. Il y a une imprégnation hormonale indubitable, qui est d’ailleurs la cause de l’apparition d’un pénis chez l’homme. Cet effet organisateur de la testostérone est vrai au niveau périphérique, mais dès qu’on dit que c’est aussi le cas dans le cerveau, les gens se mettent de nouveau à hurler. Or la testostérone qui agit au niveau des structures génitales va également différencier le cerveau. Chez l’animal, on le sait parfaitement grâce aux manipulations qui aboutissent à des résultats sexuellement différenciés au niveau morphologique. Prenez le fameux noyau préoptique du rat. Si vous traitez une femelle avec de la testostérone durant les deux semaines entourant la naissance, le noyau sera de taille mâle et cette taille importante sera irréversible pour le restant de sa vie.»
Nous sommes ici face à un exemple typique de la rhétorique dont Jacques Balthazart et ses semblables usent souvent. Par un incessant va-et-vient entre d’un côté la question de la sexuation des prédispositions comportementales humaines, et de l’autre l’évocation de données neuroanatomiques et/ou animales formulées de manière très vague, mais saupoudrée d’informations plus précises soigneusement choisies et présentées comme des exemples du mécanisme de sexuation dont il défend l’existence chez l’être humain, il s’agit de donner l’impression qu’il fait partie des « mécanismes neurobiologiques déterminant le comportement et l’orientation sexuelle » qui ont été trouvés « chez l’animal » et « qui se retrouvent mutatis mutandis dans l’espèce humaine », pour reprendre les termes qu’emploie Jacques Balthazart dans l’exposé du raisonnement circulaire qui fonde tout son discours[1].
Or si des mécanismes biologiques fondamentaux impliqués dans la sexuation du comportement animal – par exemple les diverses modalités d’action des androgènes et œstrogènes au niveau moléculaire ou cellulaire – se retrouvent effectivement dans l’espèce humaine, c’est une tout autre chose d’affirmer que les « mécanismes neurobiologiques déterminant le comportement et l’orientation sexuelle » observés « chez l’animal » s’y retrouvent (je suppose que l’absence de ‘s’ à ’sexuelle’ est une coquille, sinon c’est encore pire), ne serait-ce que parce que cette formulation laisse croire non seulement que lesdits « comportements et orientation sexuelle » se retrouvent à peu près à l’identique dans toutes les espèces animales qui ont été étudiées, mais en outre qu’ils sont toujours régis par les mêmes mécanismes, ce qui n’est absolument pas le cas.
Ce passage de l’interview de Jacques Balthazart nous amène au cœur d’une mythologie savante qu’il contribue grandement à propager, et je vais donc prendre le temps de mettre en évidence un certain nombre de faits montrant à quel point son exposé de l’état des connaissances est trompeur. Avant cela, je tiens quand même à souligner que la testostérone ne cause pas « l’apparition d’un pénis chez l’homme » : rappelons que quels que soient leurs sexes génétique et gonadique, tous les fœtus humains sont initialement dotés d’un phallus ou tubercule génital qui sauf dans certains cas d’intersexuation, se développe en prenant au final la forme typique d’un pénis en présence de testostérone et celle d’un clitoris sinon. Peut-être fallait-il informer Jacques Balthazart de l’existence de cet organe chez les femmes ? Le cas échéant, la lecture de mon article lui aura au moins servi à cela, à défaut je le crains d’ébranler ses convictions concernant la théorie à laquelle il semble si viscéralement attaché. Mais revenons aux noyaux cérébraux.
J’aurais bien aimé – cela aurait beaucoup facilité mon travail – qu’il donne la liste de cette « bonne dizaine » de tout petits noyaux humains « sexuellement différenciés » visibles uniquement « sur des coupes histologiques » et plus volumineux tantôt « chez l’homme », tantôt « chez la femme ». Surtout s’il existe des données indiquant d’une part que cette différence vient d’une action précoce de la testostérone chez les garçons, et d’autre part que leur volume influe sur des traits comportementaux différant entre femmes et hommes, puisque c’est à ce titre qu’il les invoque. Je me suis demandé s’il s’était basé sur une lecture trop rapide de la revue par Guillamon et al. (2016) de la littérature sur la recherche de corrélats cérébraux de la transidentité, qui circule depuis quelque temps et peut donner l’impression que cette bonne dizaine de noyaux existe [2], ou si c’était moi qui avais loupé quelque-chose.
Bien qu’ayant déjà examiné avec soin à plusieurs reprises depuis 2007 la littérature scientifique concernant ces noyaux, je viens donc de rafraîchir ma bibliographie pour m’assurer que je n’étais pas passée à côté d’une publication importante. Je présente dans ce qui suit une synthèse de ce qu’on sait de la différence de volume entre femmes et hommes pour tous les noyaux visibles uniquement sur des coupes histologiques ayant à ma connaissance été examinés sur ce point et parfois invoqués par des tenant∙es de thèses similaires à celle de Jacques Balthazart [3], après quelques remarques sur les noyaux étudiés chez les oiseaux chanteurs également évoqués par lui ici. Je présente pour certains noyaux des éléments complémentaires que j’ai jugés pertinents eu égard au contexte du discours de Jacques Balthazart.
De la sexuation de certains noyaux et comportements des oiseaux chanteurs
Pour mémoire, l’idée que défend Jacques Balthazart est que durant la gestation et peut-être aussi juste après la naissance (sur ce point son discours est fluctuant et reste flou), la testostérone produite par les testicules des garçons a pour effet de « masculiniser » définitivement certains noyaux cérébraux, notamment en leur conférant un volume plus grand ou plus petit que chez les filles/femmes, cela ayant in fine pour effet de « masculiniser » certains de leurs comportements – tout cela ayant été observé « chez l’animal » via des recherches étendues « dans bien des espèces » et manifestement convergentes.
Pourtant, dans son article de 1992 cité au chapitre I, Jacques Balthazart expliquait comme on l’a vu que la différence mâles-femelles dans le comportement copulatoire des oiseaux (y compris les oiseaux chanteurs tels que le canari) n’était pas due à une « masculinisation » des mâles par la testostérone (après son aromatisation en œstrogènes ou non), mais à une « démasculinisation » des femelles par les œstrogènes. Dans un récit du voyage qui l’a mené de l’observation des oiseaux à la biologie moléculaire, publié 25 ans plus tard dans une revue dont il est rédacteur en chef adjoint, il donne à ce sujet des précisions concernant un noyau « sexuellement différencié ».
Dans ce texte (Balthazart 2017), il raconte que suite aux publications de Nottebohm en 1976 et Gorski en 1978, il s’est lui-même lancé dans la course à l’identification de tels noyaux. Il a ainsi trouvé que chez la caille, un noyau situé dans la même région que celui découvert par Roger Gorski chez le rat était également plus gros chez les mâles. A ses dires, l’action sur ce noyau de la testostérone et de ses métabolites aromatisés est « nécessaire et suffisante pour activer le comportement copulatoire mâle chez la caille mâle castrée lorsqu’un stimulus sexuel femelle adéquat est présent ». Il importe de souligner, ajoute-t-il, que contrairement au noyau découvert par Gorski, « la différence de son volume entre mâles et femelles n’est pas induite par l’exposition à un environnement hormonal différent durant son ontogenèse, mais plutôt par le plus fort taux de testostérone [circulant] à l’âge adulte chez les mâles que chez les femelles ». Voilà qui diffère de la sexuation périnatale de ce noyau/comportement chez le rat.
Le dimorphisme sexué du volume des noyaux contrôlant la production des vocalisations typiques des mâles chez le canari et le diamant mandarin n’est pas non plus franchement un bon exemple de ce qu’il prétend concernant l’humain. En effet, pour reprendre les mots d’Arthur Arnold (co-auteur de la fameuse publication de Nottebohm de 1976, successeur de Gorski en 2001 à la tête du laboratoire de neuroendocrinologie de l’UCLA et poids lourd de ce domaine de recherches ayant été très actif dans la promotion de théories hormonales de la sexuation du psychisme humain), « le substrat neuronal du contrôle du chant subit des modifications morphologiques spectaculaires pendant la période d’apprentissage vocal chez les jeunes diamants mandarins mâles », et celles-ci concernent notamment « la taille des noyaux de contrôle du chant » (Bottjer et Arnold 1997). Cette caractéristique distingue ces noyaux d’autres systèmes cérébraux dont le développement est achevé assez tôt : « les régions du cerveau qui ne sont pas impliquées dans le contrôle du chant atteignent leur volume adulte vers l’âge de 25 jours, alors que les régions de contrôle du chant continuent à présenter par la suite des croissances et des régressions spectaculaires. Ainsi, des changements massifs se produisent dans le système neuronal de contrôle du chant pendant la période d’apprentissage vocal, suggérant que les influences expérientielles découlant de l’écoute et de la production de vocalisations ont amplement l’occasion d’influer sur les circuits neuronaux du chant. »
En outre, « l’administration d’androgènes à des diamants mandarins femelles nouveau-nés n’entraîne en général qu’une légère masculinisation du système du chant […] Ces résultats suggèrent que les androgènes ont des effets masculinisants sur le développement du système du chant, mais pas un rôle important. […] La version simple de l’idée de masculinisation opérée par les hormones testiculaires, issue de l’étude des mammifères, n’est pas applicable ici car la présence d’un tissu testiculaire fonctionnel ne masculinise pas le chant chez les femelles, et parce que les diverses méthodes de blocage de l’action des œstrogènes qui ont été expérimentées pour empêcher le développement masculin chez les individus de sexe génétique mâle se sont révélées relativement inefficaces » (ibidem).
Lorsque Jacques Balthazart explique dans cette interview que si on injecte de la testostérone à des femelles canari, elles vont se mettre à chanter comme des mâles et que c’est en lien avec des noyaux nettement plus volumineux chez eux, ce qu’il dit est globalement correct, mais dans ce contexte d’énonciation cela laisse croire qu’il s’agit d’un exemple de plus du mécanisme bien particulier de sexuation dont il prétend affirmer l’existence et le rôle important dans notre espèce, ce qui est donc une fois de plus trompeur.
Signalons aussi au passage qu’il existe de nombreuses espèces d’oiseaux chanteurs qui ne présentent pas de dimorphisme sexué du chant comparable à celui observé chez le canari et le diamant mandarin, ce que Jacques Balthazart sait parfaitement mais que son androcentrisme, son sexisme et/ou sa volonté de bâtir un récit simpliste de la sexuation du comportement pour mieux convaincre lui font par moment complètement oublier, comme lorsqu’il affirme que « pour un oiseau, chanter c’est attirer les femelles » et accessoirement défendre son territoire (page de son site consultée le 21 mai 2019).
Le noyau INAH-1 de l’hypothalamus
Suite à l’identification en 1978 par Roger Gorski du SDN-POA du rat (le « noyau préoptique du rat » dont parle ici Jacques Balthazart), Dick Swaab fut le premier à crier victoire dans la course à l’identification de son homologue dans le cerveau humain. Il eut ainsi les honneurs de Science en rapportant avec Eric Fliers en 1985 la toute première observation d’un « groupe de cellules sexuellement dimorphique » dans le cerveau humain, un noyau situé comme chez le rat dans l’aire préoptique de l’hypothalamus antérieur, et qu’il appellera SDN comme celui du rat. Le résumé de l’article annonce de manière définitive que ce noyau est 2.5 fois plus gros chez les hommes que chez les femmes : « the volume of this nucleus is 2.5 +/-0.6 times […] as large in men as in women ».
Cependant, la lecture de l’article permet de voir que cette affirmation générale n’était basée que sur l’examen des cerveaux conservés dans le formol de 13 hommes et 18 femmes, âgés de 10 à 93 ans au moment du décès (une bien vaste plage d’âges pour un si petit échantillon, surtout que les sujets des deux sexes n’étaient pas appariés par âge), dont on ne savait rien de la vie ni de la cause de décès (à part qu’un homme et deux femmes avaient reçu le diagnostic de maladie d’Alzheimer).
L’observation faite dans cette étude pionnière, fragile à plus d’un titre, n’a pas été répliquée par une autre équipe. Au contraire, les trois autres études indépendantes ayant examiné la taille de ce noyau et ayant été publiées ont rapporté une absence de différence statistiquement significative entre femmes et hommes. Il s’agit tout d’abord d’Allen et al. 1989, rapportant les résultats d’une étude dirigée par Roger Gorski (signalons que Melissa Hines, future figure importante de la recherche de trace de sexuation innée des prédisposition cognitives et comportementales humaines, co-signe cet article). L’équipe de Gorski forge à cette occasion l’acronyme neutre INAH-1, qui remplacera « SDN » proposé par Swaab dès lors qu’il semble finalement que ce n’est pas un « noyau sexuellement dimorphique ». Les deux autres études sont celles de LeVay (1991) et de Byne et al. (2001), confortant Byne et al. (2000) sur un échantillon légèrement étendu.
Swaab a par la suite continué à affirmer que ce noyau dont on ignore la fonction présentait un dimorphisme, arguant que les autres ne l’avaient pas trouvé du fait d’échantillons biaisés en termes d’âge. En effet, selon lui ce dimorphisme se développe uniquement après l’âge de 5 ans, disparaît à partir de 50 ans et réapparaît après 75 ans, ou bien « disparaît au-delà de l’âge de 45 ans » sans pour autant que la ménopause ait un effet sur le volume de ce noyau (Bao & Swaab 2011 ; Garcia-Falgueras et al. 2011).
Etant donné l’absence de réplication indépendante de ce résultat obtenu sur un petit échantillon de convenance[4], ainsi que l’existence a contrario de trois études négatives indépendantes publiées, il est pour le moins trompeur de parler comme le fait ici Jacques Balthazart de premier noyau dimorphique « trouvé », comme si ce dimorphisme était établi. Même l’article de Guillamon et al. (2016), pourtant généreux en dimorphismes présumés, signale que la différence de volume d’INAH-1 est « controversée » (en ne citant pas d’autre résultat positif que celui de Swaab et Fliers de 1985).
Citer ce noyau dans ce contexte, c’est-à-dire à l’appui de la théorie de la sexuation périnatale (et définitive) du cerveau, est d’autant plus malhonnête sachant ce qui est dit de l’apparition tardive de ce dimorphisme supposé et de sa variation au cours de la vie dans les seules publications soutenant son existence.
Le noyau INAH-2 de l’hypothalamus
Dans leur étude n’ayant pas retrouvé la différence concernant INAH-1, Allen et al. (1989) déjà cités identifient trois autres noyaux dans le lobe antérieur de l’hypothalamus, et rapportent que le deuxième, baptisé par elle∙eux INAH-2, est en moyenne deux fois plus volumineux chez les hommes. Elles et ils constatent aussi que son volume présente des variations considérables : rien que dans leur échantillon de seulement 11 femmes, il y a déjà un rapport de 1 à 10 entre le minimum et le maximum trouvés.
Allen et collègues soulignent qu’il était en moyenne 3.7 fois plus gros chez les femmes non ménopausées que chez les sept femmes ménopausées et la préadolescente de leur échantillon, et que si elle était confirmée, leur observation amènerait à conclure qu’INAH-2 est de même volume en moyenne entre hommes et femmes non ménopausées. Cela suggèrerait à mon sens que la taille de ce noyau varie en fait selon l’activité des gonades plutôt que selon le sexe, ce qui n’aurait rien d’étonnant connaissant le rôle que joue cette région de l’hypothalamus dans la régulation de l’axe gonadotrope, le système qui régule la production des gamètes et des hormones testiculaires et ovariennes.
Bien que certain∙es scientifiques aient affirmé sur la base de cette étude de 1989 que le volume d’INAH-2 était sexuellement dimorphique, ce constat supposé fait sur 22 sujets seulement n’a pas été répliqué par une autre équipe. Au contraire, LeVay 1991 ainsi que Byne et al. 2000/2001 déjà cités rapportent une absence de différence statistiquement significative du volume d’INAH-2 entre femmes et hommes dans leurs échantillons. Même la revue de la littérature de Guillamon et al. (2016) indique que le « pattern normatif de dimorphisme sexuel » d’INAH-2 est « M=F ».
Bref, j’espère que Jacques Balthazart ne prétend pas qu’il fait partie des noyaux dont on sait qu’ils sont plus volumineux « chez l’homme ».
Le noyau INAH-3 de l’hypothalamus
Allen et al. (1989) déjà cités, qui ont identifié et baptisé le noyau INAH-3[5], ont trouvé dans leur échantillon que celui-ci était en moyenne presque trois fois plus gros chez les hommes. L’observation d’une différence moyenne de volume d’INAH-3 a également été faite par LeVay (1991) et Byne et al. (2000/2001) déjà cités, ainsi que par García-Falgueras et Swaab (2008), toujours dans le sens H>F. Aucune observation contraire n’a été publiée, et la différence observée entre la moyenne des femmes et celle des hommes était très nette dans chacun de ces quatre échantillons indépendants. Il ne paraît donc pas déraisonnable à ce stade de penser que le noyau INAH-3 est en moyenne plus volumineux chez les hommes que chez les femmes.
Soulignons cependant que le volume de ce noyau peut difficilement être qualifié de dimorphique étant donné son extrême variabilité y compris à l’intérieur de chaque groupe de sexe, INAH-3 étant même jugé absent chez certaines femmes et certains hommes, comme l’illustre le diagramme ci-dessous tiré de García-Falgueras et Swaab 2008.
Précisons aussi que pour l’évaluation du « dimorphisme normal » (i.e. en excluant les sujet trans ou homosexuels inclus dans certaines de ces études pour voir s’ils échappaient à cette normalité supposée), ces quatre études portent en tout sur seulement 134 sujets, tous morts aux Etats-Unis ou aux Pays-Bas. En outre, l’estimation manuelle très subjective, post-mortem, de la taille de ce noyau aux contours excessivement flous (voir ici à quoi cela ressemble), varie aussi selon le procédé de coloration utilisé pour le mettre en évidence. Enfin, on remarque que la taille estimée de la différence moyenne s’est réduite depuis l’étude princeps et a tendu à diminuer à mesure que les échantillons ont grossi : le rapport entre la moyenne des hommes et celle des femmes chez les sujets présumés hétérosexuels et non trans est de 2.81 pour Allen et al. 1989 (n=22), 2.14 pour LeVay 1991 (n=22), 1.93 pour Garcia-Falgueras et Swaab 2008 (n=25) et 1.66 pour Byne et al. 2001 (n=65). La taille de la différence moyenne entre femmes et hommes n’est donc pas précisément établie.
Cette différence pourrait en particulier très bien s’avérer variable selon la classe d’âge ou les populations, et aussi – de manière plus intéressante pour le sujet qui nous occupe ici – selon le vécu des individus. C’est en effet ce que pourrait indiquer l’étude de LeVay (1991), qui a trouvé dans son petit échantillon comprenant 18 hommes « homosexuels » et 1 homme « bisexuel » morts du SIDA (j’emploie des guillemets car il y a mille et une manière de définir ces termes, et on ne sait pas à quelle définition correspondent les sujets de cette étude) que le volume d’INAH-3 était en moyenne réduit chez eux par rapport à la moyenne de 16 hommes présumés hétérosexuels (dont 6 morts du SIDA). Simon LeVay, un chercheur gay militant qui a été un très important promoteur de la théorie de l’innéité de l’homosexualité masculine en tant qu’outil de lutte contre l’homophobie[6], privilégie quant à lui l’interprétation préférée par Jacques Balthazart. Mais Byne et al. (2001), qui ont aussi trouvé une tendance à la réduction du volume d’INAH-3 quoique non statistiquement significative dans leur petit échantillon comprenant 15 hommes « homosexuels » séropositifs, mettent pour leur part en avant une possible influence du vécu. Byne et ses collègues soulignent aussi que les différences moyennes de volume observées dans leur échantillon n’avaient pas la même origine entre femmes et hommes hétérosexuels qu’entre hommes homosexuels et hétérosexuels (une différence du nombre de neurones dans le premier cas, pas dans le second). A ce jour, aucune étude publiée n’est venue confirmer le lien entre INAH-3 et orientation sexuelle ni trancher entre les diverses interprétations possibles des observations de LeVay et du groupe de Byne.
Malgré cela, c’est semble-t-il sur cette base – prise pour acquise, dichotomisée abusivement et librement interprétée comme révélant que la région de l’hypothalamus « dévolue aux comportements d’approche sexuelle » est « deux fois plus importante chez l’homme que chez la femme » – que Jean-François Marmion avait naturalisé dans Sciences Humaines en 2010 un surplus masculin de désir et de motivation à enclencher lesdits comportements (en se fondant sur la prose de Sébastien Bohler)[7].
C’est explicitement aussi sur la base des données concernant INAH-3 que dans l’affligeante vidéo de vulgarisation scientifique critiquée par moi en 2017, il était affirmé que son volume était fixé in utero et déterminait l’orientation sexuelle, de sorte que les hommes étaient habituellement attirés par les femmes parce que leur testostérone prénatale avait fait gonfler ce noyau, et les femmes par les hommes parce qu’en l’absence de testostérone prénatale ce noyau était resté petit chez elles.
Pourtant, contrairement à ce que laissent penser ces récits dont de nombreux avatars circulent depuis bientôt 30 ans dans les médias et la littérature grand public, revivifiés dans l’espace public francophone avec la publication de Biologie de l’homosexualité par Jacques Balthazart en 2010, la fonction d’INAH-3, de même que les conséquences fonctionnelles éventuelles des différences de son volume, restent à ce jour inconnues. Simon LeVay a argué que le volume d’INAH-3 pourrait être associé à l’orientation sexuelle et Dick Swaab qu’il pourrait l’être à la transidentité (sur la base de García-Falgueras et Swaab 2008 restant à répliquer), mais les données disponibles ne permettent de considérer comme établie ni l’une ni l’autre de ces associations, et encore moins l’existence d’un lien de causalité dans le sens d’un effet de ce volume sur ces traits psycho-comportementaux.
Simon LeVay a lui-même écrit dans son livre de 2010 que l’association entre l’orientation sexuelle et la taille de ce noyau restait à confirmer par d’autres études (voir note [5] de cet article de 2012), or depuis 2010 aucune étude n’est venue le faire (et LeVay a laissé cette phrase inchangée dans la seconde édition de son livre, parue en 2017). Dans Biologie de l’homosexualité, Jacques Balthazart trompait son lectorat en faisant comme si l’association avec l’orientation sexuelle et celle avec la transidentité étaient établies, mais il admettait au moins que les données disponibles ne faisaient que « suggérer » la « masculinisation inappropriée chez l’homme homosexuel » de ce noyau (p.213), affirmant ailleurs : « la taille réduite du SDN-POA des homosexuels peut, à la lumière des études animales, être considérée comme le résultat d’une déficience de masculinisation embryonnaire qui induirait en parallèle la taille réduite du noyau » (p. 266) – on appréciera au passage le charmant vocabulaire de cet homme hétérosexuel affiché qui prétend lutter contre l’homophobie. Il admettait aussi qu’on ne savait pas si son « petit volume […] chez les transsexuels H->F représente la cause ou la conséquence de l’identité sexuelle inversée ou si les deux sont le reflet d’un troisième facteur […] inconnu » (fin du chapitre 13) – on appréciera aussi la délicatesse du vocabulaire qu’il utilise pour parler des personnes transgenres, outre sa substantivation des termes « homosexuels » et « transsexuels », caractéristique des personnes ayant une vision binaire et essentialiste du genre.
Par ailleurs, alors que Jacques Balthazart use sans vergogne du terme « SDN-POA » pour désigner INAH-3 dans ses écrits de vulgarisation (comme on vient d’en voir un exemple), ce n’est pas ainsi qu’il est désigné dans la littérature scientifique car son homologie avec le SDN-POA du rat n’est pas du tout établie. L’idée qu’il s’agit du meilleur candidat pour cette homologie, dans l’hypothèse où il existerait un homologue humain au SDN-POA du rat, ne fait même pas consensus. Ainsi, Swaab estime que davantage d’arguments plaident en faveur de l’hypothèse qu’INAH-1 est l’homologue du SDN-POA (voir dans Garcia-Falgueras et al. 2011), et affirme encore par exemple dans Olvera-Hernandez et al. 2017 que la question de l’homologie du SDN-POA reste ouverte. On peut aussi noter que Guillamon et al. (2016) désignent INAH-3 sous ce seul nom, signalant en revanche qu’INAH-1 a été appelé SDN par Swaab.
Il faut également souligner que contrairement à ce que Jacques Balthazart a affirmé avec Peggy Sastre, Franck Ramus, Claudine Junien, Nicolas Gauvrit, Michel Raymond et deux autres allié∙es de circonstance dans leur défense de la vidéo grotesque évoquée plus haut suite à ma critique, on ne saurait dire que le « noyau sexuellement dimorphique de l’aire préoptique (INAH3 pour les spécialistes) […] est de taille féminine chez les hommes homosexuels ». En effet, outre qu’on serait bien en peine de dire qu’elle est la « taille féminine » de ce noyau étant donné son immense variabilité, « même si c’était vrai » (que la taille d’INAH-3 a un lien avec l’orientation sexuelle, car encore une fois les données disponibles ne permettent pas de l’établir), « il est peu probable que la taille d’INAH-3 soit un facteur clé de régulation de l’orientation sexuelle. En effet, il y aurait trop d’exceptions (des hommes homosexuels avec un gros INAH-3 et des hommes hétérosexuels avec un petit INAH-3) pour qu’il soit possible de croire que la taille d’INAH-3 est cruciale » : ce n’est pas moi qui le dis, mais Bailey et al. (2016) dans un article que Jacques Balthazart et ses soutiens ont pourtant osé citer à l’appui de leurs dires. Les échantillons des études publiées sur le sujet contiennent effectivement nombre d’hommes hétérosexuels ayant un noyau de volume mesuré plus proche de la moyenne des femmes (voire égal à 0), et inversement d’hommes homosexuels ayant un noyau de volume plus proche de la moyenne des hommes hétérosexuels voire supérieur à celle-ci.
Dispose-t-on au moins de données convergentes et convaincantes indiquant que le mécanisme de sexuation périnatale du SDN-POA du rat et du comportement sexuel associé « se retrouvent mutatis mutandis dans l’espèce humaine » au niveau du noyau INAH-3 et de l’orientation sexuelle, à laquelle Jacques Balthazart soutient que ce noyau est associé ? C’est très loin d’être le cas, et ce au moins à deux titres.
Premièrement, aucune des études génétiques de l’orientation sexuelle menées jusqu’à ce jour n’a pointé vers une association avec un gène de la voie androgénique, ce qui devrait quand même faire réfléchir, et lorsqu’on examine avec soin et rigueur les résultats de la recherche menée sur l’être humain par d’autres méthodes comme l’a fait dans son livre Rebecca Jordan-Young (2016 [2010]), on ne peut que conclure qu’ils ne laissent tout au plus la place qu’à l’existence d’effets modestes, non déterminants, de le testostérone prénatale sur cette dimension du psychisme humain comme sur d’autres. Il me paraît assez significatif que Marc Breedlove, un pionnier avec Arthur Arnold de la recherche sur la masculinisation du substrat de certains comportements par la testostérone (voir Breedlove et Arnold 1980), ait écrit ceci récemment : « Il est clair que d’autres facteurs que les androgènes prénataux ont une influence sur la différenciation sexuelle du cerveau humain […] La grande question est de savoir si les stéroïdes gonadiques prénataux ont conservé la moindre influence sur le comportement humain […] Nous ne savons pas si la plupart des gens sont hétérosexuels parce que les femmes n’ont pas été exposées à un taux élevé de testostérone avant la naissance, tandis que les hommes l’ont été, ou si c’est parce qu’ils ont été socialisés pour être ainsi […] Il est peut-être temps d’abandonner l’idée que les hommes gays sont sous-masculinisés » (Breedlove 2017).
Deuxièmement, on sait déjà que la théorie généralement admise par les biologistes concernant la sexuation périnatale du SDN-POA du rat est inapte à expliquer la sexuation du substrat de l’orientation sexuelle humaine. En effet, l’idée est que si ce noyau du rat est beaucoup plus gros chez les mâles, c’est à cause d’effets de l’œstradiol issu de la conversion locale (dans le cerveau) de la testostérone mise en circulation par leurs testicules pendant une période critique du développement du cerveau (Jacques Balthazart affirme dans Biologie de l’homosexualité que divers arguments démontrent « de façon péremptoire » que ça se passe ainsi « chez le rat tout au moins »), or des données solides et convergentes pointent clairement vers la conclusion que ça ne se passe pas ainsi dans notre espèce, comme le défend par exemple David Puts (Motta-Mena et Puts 2018), qui loin d’être un critique de la théorie hormonale de la sexuation des comportements humain est un acteur important de ce champ de recherches.
Il y a d’abord et surtout le cas des personnes de caryotype 46,XY pourvues de testicules fonctionnels mais dites complètement insensibles aux androgènes, car porteuses d’une mutation génétique les privant de récepteurs aux androgènes fonctionnels. Chez ces personnes dont l’anatomie apparente est parfaitement féminine (et même plus, la testostérone et ses dérivés androgéniques n’ayant pas chez elles les effets présents chez les femmes 46,XX), et qui sont pour cette raison assignées au sexe féminin à la naissance, élevées en tant que filles et perçues sans ambiguïté comme telles, l’aromatase et la voie œstrogénique fonctionnent normalement. Si les choses se passaient comme chez le rat, elles devraient donc avoir une orientation sexuelle (et bien d’autres traits psychologiques) typique de celles des hommes 46,XY. Il s’avère qu’elles ont au contraire une orientation sexuelle (et une identité de genre, entre autres) typique de celle des femmes. Ce fait bien documenté et relevé depuis longtemps par des chercheur∙es du domaine (par exemple par Roger Gorski en 2000[8]) montre que l’éventuel mécanisme biologique de contrôle hormonal de la sexuation de l’orientation sexuelle humaine diffère nécessairement de celui trouvé chez ce modèle animal ou qu’il est de poids absolument négligeable dans la détermination de l’orientation sexuelle, comparé à celui de la socialisation ou à celui d’une action directe des androgènes sur son substrat, les deux interprétations étant possibles.
D’autres données vont dans le même sens, telles celles de l’étude de gène candidat dirigée par Dean Hamer ayant échoué à trouver une corrélation entre la variation de l’orientation sexuelle masculine et celle du gène codant pour l’aromatase, qui induit pourtant une variation de la capacité d’aromatisation de la testostérone en œstradiol (DuPree et al. 2004). Cette étude n’a pas été répliquée, mais son résultat est conforté par l’absence de signal pointant vers ce gène dans les études de liaisons et études pangénomiques ultérieures. Ses auteurs signalent en outre que dans les cas documentés à leur connaissance d’hommes 46,XY porteurs d’une mutation délétère de ce gène (incapables d’aromatiser la testostérone), ceux-ci avaient une orientation sexuelle typiquement masculine (hétérosexuelle). Dans la liste des 14 rapports de tels cas que Cooke et al. (2017) ont pu retrouver, pour 6 une orientation sexuelle hétérosexuelle est explicitement rapportée, et pour les autres soit un « comportement sexuel » (ou « développement sexuel » et/ou « libido ») « normal » l’est, soit rien n’est signalé. Allant encore dans le même sens, la plus grosse étude jamais réalisée sur les femmes exposées in utero au Distilbène (Titus-Ernstoff et al. 2003), portant sur plusieurs milliers d’entre elles, a trouvé que malgré leur exposition à ce puissant composé œstrogénique atteignant le cerveau, une mesure indicative de leur orientation sexuelle n’était pas plus gynophile que ce qu’on observe habituellement chez les femmes (de petites études antérieures portant en tout sur quelques dizaines de femmes ont suggéré que l’orientation bi- ou homosexuelle pourrait être plus fréquente chez elles, mais sont de maigre poids face à celle-ci).
En bref, si d’aventure la sexuation de l’orientation sexuelle humaine est notablement influencée in utero ou peu après la naissance par un mécanisme hormonal, il est clair que ce mécanisme n’est pas celui qui est à l’œuvre dans la sexuation du SDN-POA du rat, dont Jacques Balthazart laisse croire dans cette interview qu’il fait partie des « déterminismes biologiques de contrôle de la différenciation des sexes qui se sont développés et ont été sélectionnés pendant 3,5 milliards d’années », des déterminismes dont on imagine mal comment ils auraient pu « subitement disparaître chez l’humain ». Certes, une fois ces déterminismes présentés ainsi, c’est-à-dire comme ayant été sélectionnés dans tout le vivant voire déjà présents il y a 3,5 milliards d’années (!), leur disparition « subite », et ce uniquement dans l’espèce humaine, ne paraît pas très plausible. Il s’agit d’un élément de rhétorique classique chez les semblables de Jacques Balthazart – voir par exemple dans cet article de 2012 mon analyse d’une interview par Peggy Sastre (déjà) dans laquelle Michel Raymond expliquait : « Les cerveaux sont biologiquement différents vu que les forces sélectives agissant sur les mâles et sur les femelles ne sont pas les mêmes, ce qui fait que les comportements sélectionnés depuis des centaines de millions d’années sont, eux aussi, différents. ».
Il faut d’ailleurs signaler, pour en finir sur ce sujet du SDN-POA en lien avec la théorie de la sexuation hormonale de l’orientation sexuelle, que même parmi les mammifères, les données animales n’offrent déjà pas un panorama unifié – outre que chez le rat, le lien de causalité entre volume du SDN-POA et sexuation des préférences pour un partenaire sexuel femelle vs mâle n’est pas aussi simple et clair que ce que laisse croire Jacques Balthazart[9], et que contrairement à ce qu’il a écrit dans Biologie de l’homosexualité, il n’est pas exact qu’une fois la taille du SDN-POA « déterminée à la fin de la première semaine de vie postnatale, elle est fixée pour le reste de la vie » (p. 83) et la préférence de partenaire avec[10].
Le consensus scientifique actuel concernant la sexuation périnatale hormonale du substrat de certains comportements chez les primates non humains, ou tout au moins chez le macaque rhésus (l’espèce étudiée sur laquelle ce consensus est pour l’essentiel fondé), est que cette sexuation lorsqu’elle existe ne repose pas sur le mécanisme biologique si central chez le rat de masculinisation périnatale par l’œstradiol issu de l’aromatisation de la testostérone. Dans un article récent, Dick Swaab écrit ainsi non seulement que dans les espèces à gestation de longue durée et à gros cerveau, la période critique de sexuation hormonale survient plus tôt que chez les rongeurs (ne se poursuivant en particulier pas péri- ou post-natalement selon lui), mais aussi que « les cerveaux des primates semblent être masculinisés sans passer par l’aromatisation de la testostérone » (Graïc et al. 2018). Margaret McCarthy, autre poids lourd de la recherche de différences cérébro-comportementales innées entre femmes et hommes (qu’elle explore quant à elle chez la souris), promotrice influente de thèses similaires à celle de Jacques Balthazart, va même jusqu’à affirmer sans ambages en 2016 : « chez les rongeurs, les androgènes produits par les testicules sont aromatisés en œstrogènes, une étape essentielle du processus de masculinisation, tandis que chez les primates les androgènes agissent directement ». Jacques Balthazart ne l’ignore évidemment pas (voir par exemple dans Bakker et al. 2006 dont il est co-auteur) [11], et sait donc que ce mécanisme biologique proximal de sexuation de certains substrats du comportement « sélectionné pendant 3,5 milliards d’années » chez les rongeurs a été « remplacé » par un autre mécanisme « sélectionné pendant 3,5 milliards d’années » chez les primates.
Par ailleurs, alors que tout le discours de Jacques Balthazart est orienté par sa profonde conviction que la sexuation assez nette du choix de partenaires sexuels observée dans les sociétés humaines résulte comme chez la caille ou le rat d’un déterminisme biologique, et en aucune façon de la très forte contrainte socio-culturelle à la binarité de genre et à l’hétérosexualité qui les caractérise, je remarque pour ma part que chez certains primates, ce qui s’approche le plus de la notion proprement humaine d’orientation sexuelle est parfois bien moins nettement sexué que chez nous.
L’exemple du bonobo, notre plus proche cousin avec le chimpanzé commun, est suffisamment connu pour que je ne m’étende pas dessus. Dans cette espèce, tous les individus peuvent être dits « bisexuels » au sens où ils se livrent à des copulations avec des individus des deux sexes, et ce y compris en présence de congénères du sexe opposé motivés ou réceptifs. Que ce soit difficile à imaginer ou non, un mécanisme neurobiologique fondamental de sexuation de la « préférence » pour le sexe opposé semble bel et bien avoir largement « disparu » dans cette espèce.
Mais je sais que ce contre-exemple n’est pas suffisant pour convaincre les biologistes à œillères qui comme Jacques Balthazart ou Michel Raymond, ne peuvent concevoir qu’une chose similaire se soit produite dans notre espèce. Lors d’une conversation informelle, un de leurs semblables m’a ainsi opposé que le caractère exceptionnel des mœurs sexuelles du bonobo démontrait qu’une telle évolution avait eu une très faible probabilité de se produire, et qu’il était donc parfaitement improbable qu’une évolution similaire se soit produite une deuxième fois, en l’occurrence dans la lignée humaine. L’exception confirmerait la règle, et donc l’improbabilité radicale d’une autre exception à celle-ci. La force d’une conviction peut mener à de beaux sophismes…
D’autres espèces de primates ont des comportements sexuels moins rigidement sexués que les nôtres, tels le macaque rhésus chez qui la monte d’un congénère, de même que la présentation de son postérieur pour initier ou accepter celle-ci, est couramment le fait d’individus des deux sexes y compris vis-à-vis de congénères du même sexe, l’ampleur voire l’existence de la différence entre les sexes dans la fréquence de ces divers comportements s’avérant aussi dépendre beaucoup du contexte social (comme le signalent Thornton et al. 2009, bien qu’étayant solidement l’hypothèse de l’organisation prénatale par la testostérone de certains de ces comportements dans cette espèce).
Un autre exemple abondamment documenté depuis plusieurs décennies s’approche davantage de la bisexualité humaine. Plutôt que de préférer les partenaires sexuels d’un sexe ou de l’autre (comme c’est le plus souvent le cas dans les sociétés humaines), ou d’avoir des activités sexuelles avec des partenaires des deux sexes mais souvent en lien avec des motivations sociales spécifiques (comme chez le macaque rhésus ou le bonobo), dans certaines populations de macaque japonais, une large proportion des femelles ont des activités homosexuelles comme hétérosexuelles qui semblent déconnectées de toute motivation sociale, et préfèrent certaines femelles à certains mâles et inversement (Vasey et al. 2014). Signalons au passage que Vasey et Pfaus (2005) ont trouvé que chez ces femelles qui couramment en sollicitent sexuellement d’autres, les montent, exercent à leur contact des poussées pelviennes, entrent en compétition avec des mâles pour accéder à des femelles et préfèrent certaines femelles à certains mâles, le volume du noyau AHdc n’était pas augmenté, or pour William Byne, l’auteur de la seule étude ayant partiellement répliqué l’observation de LeVay (1991) concernant un possible lien entre INAH-3 et orientation sexuelle, le noyau AHdc du macaque rhésus est probablement l’homologue du SDN-POA du rat (Byne 1998).
En synthèse, si le noyau INAH-3 semble être en moyenne plus volumineux chez les hommes que chez les femmes au moins dans certaines sous-populations, affirmer qu’il est plus volumineux « chez l’homme » est trompeur – outre que compte tenu de ce que Jacques Balthazart prétend par ailleurs, cela nécessite de considérer que « l’homme homosexuel », pour reprendre son vocabulaire, n’est pas vraiment un homme.
De manière plus générale, nombre d’assertions faites concernant INAH-3 par Jacques Balthazart lorsqu’il s’adresse au grand public sont fallacieuses voire démenties par la littérature scientifique. Celle-ci ne plaide pas particulièrement en faveur de la thèse qu’il défend, et on sait en particulier déjà que l’éventuel mécanisme (neuro)biologique de sexuation d’aspects du comportement sexuel dont il prétend qu’ils sont associés à la sexuation de ce noyau n’est pas celui connu chez les rongeurs, qu’il décrit dans ses conférences à l’appui de cette thèse. L’existence même d’une influence notable de la testostérone périnatale sur l’orientation sexuelle masculine, censée être liée à un effet de celle-ci sur la taille d’INAH-3, est considérée comme douteuse y compris par des leaders de la recherche dans ce domaine.
Le noyau INAH-4 de l’hypothalamus
Allen et al. (1989) déjà cité, ayant rapporté pour la première fois l’existence des noyaux INAH-2 à 4, rapporte une absence de différence significative entre femmes et hommes pour le volume d’INAH-4.
LeVay (1991), Byne et al. (2001/2000) et García-Falgueras et Swab (2008) déjà cités ont également conclu à l’absence de différence significative de volume, et aucune autre étude sur les différences de volume d’INAH-4 entre femmes et hommes n’a été publiée à ma connaissance.
Je suppose et espère donc que Jacques Balthazart ne prétend pas qu’INAH-4 est « plus volumineux chez l’homme » ou « chez la femme ».
Le noyau supraoptique de l’hypothalamus (SON)
Le noyau supraoptique de l’hypothalamus est principalement constitué de neurones produisant de la vasopressine et de neurones produisant de l’ocytocine, qu’ils relâchent dans la circulation générale via l’hypophyse.
Dans la petite étude d’Allen et al. (1989) déjà citée, menée sur 11 femmes et 11 hommes décédés appariés par âge, le volume du noyau supraoptique a également été étudié, et l’article rapporte une absence de différence statistiquement significative.
Dans Ishunina et Swaab 1999, résultant d’une étude menée sur 15 hommes et 17 femmes âgés de 29 à 94 ans au moment de leur décès, il est rapporté une absence de différence statistiquement significative entre eux dans la taille des neurones à vasopressine comme dans celle des neurones à ocytocine du noyau supraoptique.
Je n’ai pas trouvé d’étude(s) permettant d’établir que ce noyau est plus volumineux « chez l’homme » ou « chez la femme », et espère donc ici encore que Jacques Balthazart ne prétend pas qu’il fait partie de la bonne dizaine de noyaux « sexuellement différenciés » connus pour différer par leur volume chez l’être humain.
Le noyau du lit de la strie terminale (BST ou BNST)
Le noyau du lit de la strie terminale interconnecte l’amygdale à l’hypothalamus et diverses autres structures cérébrales. Il est connu pour son implication dans la réponse au stress et les états d’anxiété.
Dans une étude dirigée par Roger Gorski, Melissa Hines trouve en 1985 dans un échantillon de 32 cochons d’Inde adultes qu’une partie formant une tache sombre (sur les coupes histologique après coloration) dans la partie postéro-médiale de ce noyau est environ 36% plus volumineuse chez les mâles (Hines et al. 1985). Suite à cela, peu après leur publication sur les noyaux interstitiels et supraoptique de l’hypothalamus humain, Roger Gorski publie avec sa collaboratrice Laura Allen une observation concernant cette même région chez l’être humain.
Allen et Gorski (1990) rapportent que dans leur échantillon de 13 femmes et 13 hommes décédés appariés par âge, le volume de la « région postéro-médiale du noyau du lit de la strie terminale formant une tache sombre » est en moyenne 2.47 fois plus grand chez les hommes. Suggérant de baptiser cette région « BNST-dspm » (pour « darkly staining posteromedial component of the bed nucleus of the stria terminalis »), elle et il suggèrent que comme chez le cochon d’Inde, ce « dimorphisme sexuel » pourrait être influencé par les hormones gonadiques et pourrait partiellement sous-tendre un fonctionnement « sexuellement dimorphique » dans le comportement agressif et/ou sexuel.
Je n’ai pas trouvé de trace de réplication de cette étude.
Cinq ans plus tard, dans Zhou et al. 1995, dans le cadre de la recherche de l’origine de ce qu’il appelle la transsexualité (caractérisée ici par le fait d’avoir « le fort sentiment, souvent dès l’enfance, d’être né du mauvais sexe »), le groupe de Dick Swaab rapporte une différence entre les sexes du volume du centre du noyau du lit de la strie terminale qu’il désigne par l’acronyme BSTc. Swaab et ses collaborateurs rapportent dans la prestigieuse revue Nature que dans leur échantillon de 36 sujets décédés présumés non trans, le BSTc était en moyenne 40 % plus gros chez les hommes présumés hétérosexuels que chez les femmes présumées hétérosexuelles (61 % chez ceux identifiés comme homosexuels). De plus, ils rapportent que le volume de cette région du noyau était en moyenne encore plus petit chez les six sujets trans MtF de leur échantillon (25 % plus petit que chez les femmes résumées hétérosexuelles), bien que la différence n’atteigne pas le seuil de significativité statistique. Après avoir argué que le noyau du lit de la strie terminale « joue un rôle essentiel dans le comportement sexuel masculin » (et dans la régulation de la sécrétion de GnRH), « comme l’ont montré les études faites chez le rat », ils estiment que bien qu’il n’existe aucun indice direct de l’existence d’un rôle similaire dans le comportement sexuel humain, leurs résultats « indiquent que ce noyau est peut-être impliqué dans les fonctions sexuelles ou reproductives humaines ». Ils soulignent également que ce volume n’était pas plus petit chez les hommes homosexuels mais l’était y compris chez les deux « transexuels à survenue tardive », ce qui indique à leurs yeux que cette taille réduite est liée à « l’altération de l’identité de genre en soi » plutôt qu’à l’âge auquel elle devient apparente, et est sans rapport avec l’orientation sexuelle. Pour eux, leurs observations « étayent l’hypothèse que le développement de l’identité de genre résulte d’une interaction entre les hormones sexuelles et le cerveau en développement ».
En 2000, l’équipe de Dick Swaab encore rapporte dans une revue d’endocrinologie une différence similaire sur un échantillon de 28 sujets présumés non trans et non intersexués (9 hommes identifiés comme homosexuels et 19 femmes et hommes présumés hétérosexuels) dont 21 déjà inclus dans l’étude de 1995 (Kruijver et al. 2000). Trouvant comme en 1995 qu’il n’y a pas de lien statistiquement significatif entre l’orientation sexuelle masculine et la taille de ce noyau dans cet échantillon, l’équipe regroupe les 18 hommes et trouve à nouveau chez eux un volume en moyenne supérieur de 40% à celui de la moyenne des femmes, bien que le volume estimé dans les différents groupes soit presque le double de celui rapporté dans l’article de 1995 (ils l’expliquent par la modification de le technique employée, notamment l’utilisation d’un autre marqueur pour teinter les coupes histologiques). Cette fois, le volume moyen chez les 5 sujets trans MtF est quasi-identique à celui des 10 femmes, et il est chez le seul sujet trans FtM « dans la plage masculine » (en fait plus grand encore que chez tous les hommes contrôles de l’échantillon). Selon eux, leur étude « soutient clairement la théorie selon laquelle chez les transsexuel(le)s, la différenciation sexuelle du cerveau et celle des organes génitaux peuvent aller dans des directions opposées, et pointe vers l’existence d’une base neurobiologique au trouble de l’identité de genre ».
Aucune réplication indépendante de cette observation n’a été publiée.
Deux ans plus tard, sur la base de l’étude de fœtus, enfants, adolescents et adultes des deux sexes (50 sujets en tout), l’équipe de Dick Swaab toujours rapporte un résultat jugé inattendu. Partant de l’idée que la différenciation de cette région se fait chez le rat peu après la naissance sous l’effet de la testostérone, Chung et al. (2002) expliquent qu’ils s’attendaient à observer une divergence précoce des volumes entre femmes et hommes, or ils ont trouvé une absence de différence chez les fœtus et chez les enfants et adolescents, la différence H>F n’émergeant que chez les adultes de leur échantillon (âgés de plus de 22 ans). Pour moi, ce résultat ainsi que le précédent soutient tout autant voire davantage l’idée que le volume de ce noyau est modifié par l’activité gonadique (et donc aussi par les traitements hormonaux administrés aux sujets trans des échantillons de Swaab), par opposition à celle qu’il serait déterminé par le niveau périnatal de testostérone et influerait sur la formation de l’identité de genre.
Je note qu’une autre équipe ayant travaillé récemment sur le noyau de la strie terminale (mais sans étudier sa différence de volume entre femmes et hommes), bien que moins prudente à un autre endroit de l’article, écrit à un moment que le noyau du lit de la strie terminale est « peut-être » dimorphique chez l’être humain, citant pour toute référence l’étude d’Allen et Gorski sur le BNST-dspm et celle du groupe de Swaab sur le BSTc (Avery et al. 2014). Une telle prudence est compréhensible : ces deux observations non répliquées sont particulièrement fragiles étant donné les conditions de leur obtention, notamment l’utilisation de petits échantillons de convenance et la forte détermination de ces deux équipes à trouver ce type de dimorphisme.
Pourtant, dans son précédent livre, Jacques Balthazart :
– affirmait que le noyau du lit de la strie terminale jouait un rôle important « dans le contrôle du comportement sexuel chez l’animal », citant en référence deux études s’avérant faites sur des rats, et s’avérant être tout simplement les deux études de 1974 et 1976 qui étaient citées par Zhou et al. en 1995 (pourquoi se fatiguer à chercher plus loin quand il suffit de recopier ce que d’autres ont écrit 15 ans auparavant et qui flatte ses préjugés, et pourquoi embrouiller les gens avec la précision inutile que cela concerne le rat, autant l’enlever et écrire « chez l’animal » à la place, n’est-ce pas ?), et ce alors que Zhou et collègues les citaient à l’appui de l’idée que le BSTc joue un rôle essentiel dans le comportement sexuel masculin et dans la régulation de la sécrétion de GnRH (glissement fréquent chez Jacques Balthazart consistant à considérer que le comportement sexuel masculin est le comportement sexuel tout court, et suppression de la mention de la régulation de la sécrétion de GnRH pour éviter que les lecteur∙ices se demandent si les différences de tailles de ce noyau ne pourraient pas être simplement liées à des différences purement physiologiques),
– ajoutait que « chez diverses espèces », sa partie centrale était plus grosse chez les mâles « largement » du fait de l’action précoce des stéroïdes sexuels et enchaînait en affirmant tranquillement : « Ce noyau est également sexuellement différencié dans l’espèce humaine », donnant pour toute référence à l’appui l’article d’Allen et Gorski de 1990 (portant sur le BNST-dspm, pas du tout au même endroit que le BSTc), avant de broder sur les travaux de Swaab (portant sur le BSTc) pour suggérer que l’ « identité sexuelle masculine » pourrait être liée à une certaine « imprégnation hormonale […] pendant la vie embryonnaire », dont la taille de ce qu’il appelle « BNSTc » pourrait être un marqueur.
Il me semble que cela se passe de commentaires.
Quoi qu’il en soit et pour en revenir à la présente interview, on a donc ici affaire à un noyau dont on ne saurait affirmer qu’il est « plus volumineux chez l’homme », et dont les maigres observations humaines concernant la partie que Jacques Balthazart instrumentalise plus particulièrement (le BSTc) n’étayent pas particulièrement la théorie qu’il soutient.
Ces observations peuvent en effet au moins autant voire davantage soutenir qu’une différence moyenne entre femmes et hommes est le cas échéant uniquement liée à des différences strictement liées à la physiologie de la reproduction émergeant à partir de la puberté. Même Guillamon et al. (2016), bien qu’indiquant que le « pattern normatif de dimorphisme sexuel » pour le BSTc est « M>F », rappellent que Chung et al. (2002) ont estimé que ce dimorphisme prétendu n’émergeait qu’à l’âge adulte, et soulignent que les observations faites par l’équipe de Swaab sur des sujets trans sont peut-être attribuables aux effets de la thérapie hormonale de réassignation, qualifiant cette explication de « plus probable » que l’explication alternative proposée, à savoir que le BSTc de petite taille serait un marqueur spécifique du développement de la transidentité MtF « non-homosexuelle » (i.e. avec attirance pour les femmes, dans leur référentiel).
Le noyau suprachiasmatique de l’hypothalamus (SCN)
Le noyau suprachiasmatique de l’hypothalamus, connu pour sa fonction de contrôle des rythmes circadiens et pour lequel des différences de volume entre femelles et males ont été observées chez des rats et des souris, a également été étudié par Dick Swaab dans le cadre de sa recherche tous azimuts d’un dimorphisme sexué qui pourrait être mis en relation avec la propension à la « transsexualité ».
Dans Zhou et al. 1995 déjà cité, Swaab et ses collaborateurs signalent qu’ils n’ont pas trouvé qu’il satisfaisait aux deux conditions qu’ils avaient fixées, à savoir être « sexuellement dimorphique » et ne pas être « influencé par l’orientation sexuelle », renvoyant pour la documentation de ces constats à Swaab et Hofman 1995 ainsi qu’à des données non publiées par eux. Ils signalent également qu’ils n’ont pas trouvé que son volume était réduit ni augmenté chez les sujets trans présentant dans cet échantillon une différence au niveau du BSTc, précisant ne pas avoir publié ces données non plus.
Relevons au passage cet exemple de biais de publication en défaveur de résultats négatifs, un biais qui mine la recherche sur les différences entre les sexes par sa capacité à créer l’illusion que des différences existent lorsqu’elles n’existent pas, et aussi à exagérer la taille d’une différence lorsqu’on l’estime par méta-analyse des études publiées. David et al. (2018) ont montré comment de nombreuses annonces de « découvertes » de différences entre femmes et hommes (en l’occurrence dans les études de neuroimagerie fonctionnelle par IRM) pouvaient a contrario être des faux positifs, ce qui souligne encore une fois combien il est inapproprié de prendre pour acquis les résultats d’études non répliquées, surtout faites sur de petits échantillons non aléatoires.
Mais revenons à Swaab et Hofman (1995) et à la recherche d’une différence entre femmes et hommes pour le noyau suprachiasmatique. Swaab et son collaborateur écrivent qu’ils n’ont pas trouvé de différence pour la subdivision de ce noyau contenant des neurones à vasopressine, mais qu’ils ont trouvé celle contenant des neurones à peptide vasoactif intestinal deux fois plus grosse chez des hommes âgés de 10 à 30 ans que chez des jeunes femmes, cette différence s’inversant entre 41 et 65 ans puis disparaissant après 65 ans ; ils rappellent aussi qu’ils avaient trouvé en 1990 que la subdivision du noyau suprachiasmatique contenant des neurones à vasopressine était deux fois plus grosse chez des hommes homosexuels que chez des hommes hétérosexuels, mais Swaab a rapporté en 1993 que la lésion de ce noyau chez le rat mâle ne perturbait pas leur « orientation sexuelle », et dans un autre article en 1993 que ce noyau était 2.5 plus gros en octobre-novembre qu’en mai-juin, or rien n’indique que les femmes, hommes hétérosexuels et hommes homosexuels de leurs autres études ont été appariés par mois du décès.
Je relève aussi que dans la plus récente publication que j’ai pu trouver sur le sujet (Graïc et al. 2018), Swaab et ses co-auteurs listent cinq caractéristiques du noyau suprachiasmatique distinguant selon eux certaines espèces de mammifères d’autres espèces du même groupe : 1. distinguant l’opossum des autres mammifères étudiés ; 2. distinguant l’humain des autres mammifères étudiés ; 3. distinguant la vache du chameau et de l’humain ; 4. distinguant les bovins de la souris ; 5. distinguant le cheval de « la plupart des mammifères ». Dans cette étude, ils rapportent en particulier que chez des bovins, le volume total des neurones à peptide vasoactif intestinal de ce noyau était en moyenne plus grand chez les femelles que chez les mâles (+ 36 %), en sens inverse de ce qu’ils rapportent chez l’humain, le rat et la gerbille. Pour expliquer cette discordance, ils avancent que cela pourrait provenir du fait que les bovins ont été sélectionnés de sorte à favoriser la production de lait, or celle-ci « est influencée par les rythmes circadiens ». Les scientifiques qui étudient les comportements sexuels sur des modèles rats et souris de laboratoire ne se demandent a contrario jamais de quelles particularités sont porteuses les lignées de rongeurs sélectionnées pour la recherche, présentant certains avantages en termes de facilité de reproduction et/ou d’élevage.
Pour en revenir aux humains, Guillamon et al. (2016) indiquent que le « pattern normatif de dimorphisme sexuel » pour le noyau suprachiasmatique est « M=F » et précisent que ce noyau « semble être masculin chez les MtFs », citant en référence Zhou et al. 1995 (qui rapporte en fait une absence de différence entre sujets MfF et femmes et hommes non trans).
Bref, la recherche n’ayant pas montré que le noyau suprachiasmatique était plus volumineux « chez l’homme » ni « chez la femme », j’espère que Jacque Balthazart ne prétend pas qu’il l’est.
Le noyau paraventriculaire de l’hypothalamus (PVN)
Dick Swaab s’est également intéressé au noyau paraventriculaire de l’hypothalamus, un bon candidat à dimorphisme sexué car il est impliqué notamment dans la sécrétion d’une hormone nécessaire à l’accouchement et impliquée dans l’allaitement (ocytocine), dans le contrôle de l’érection (également en lien avec l’ocytocine mais via un autre groupe de neurones) et dans celui de la sécrétion par l’hypophyse d’une hormone nécessaire à la lactation (prolactine). Il contient aussi des neurones sécrétant de la vasopressine, un peptide connu dans notre espèce pour ses effets antidiurétiques et hypertenseurs, mais qui a été associé à certains comportements sexuels chez des rongeurs. Ce noyau fait également partie de l’axe corticotrope (hypothalamus-hypophyse-glandes surrénales), le système qui contrôle la réaction hormonale au stress, dans lequel diverses différences entre les sexes ont été documentées notamment chez le rat et la souris.
Comme pour le noyau suprachiasmatique, Swaab et ses collaborateurs signalent dans Zhou et al. (1995) qu’ils n’ont pas trouvé que le noyau paraventriculaire satisfaisait aux deux conditions qu’ils avaient fixées, à savoir être « sexuellement dimorphique » et ne pas être « influencé par l’orientation sexuelle », renvoyant ici à Swaab et Hofman (1995) et à des données non publiées. A la différence du noyau suprachiasmatique, il n’y a rien concernant le noyau paraventriculaire dans Swaab et Hofman (1995), et on est donc rendu à des données non publiées pour en savoir plus. Etant donné que ce noyau n’a pas été associé à l’orientation sexuelle, on peut déduire de ce qui précède que l’équipe n’a pas trouvé qu’il était « sexuellement dimorphique ».
Guillamon et al. 2016 indiquent également pour le noyau paraventriculaire que le « pattern normatif de dimorphisme sexuel » est « M=F », précisant que ce noyau « semble être masculin chez les MtFs ».
Swaab rapporte dans Ishunina et Swaab 1999, étude réalisée sur 15 hommes et 17 femmes âgés de 29 à 94 ans au moment de leur décès, l’observation que les neurones à vasopressine du noyau paraventriculaire étaient en moyenne un peu plus gros chez les hommes, uniquement dans l’hémisphère gauche (ne trouvant en revanche aucune différence pour les neurones à ocytocine), mettant ce constat en relation avec l’observation d’un taux de vasopressine dans le sang en moyenne supérieur chez les hommes (j’avais parlé en 2013 de l’instrumentalisation de cela par Boris Cyrulnik, qui prétendait que « la vasopressine est une neurohormone sécrétée plutôt par les hommes, qui les encourage plutôt à passer à l’action » – l’opposant à l’ocytocine sécrétée surtout par les femmes, qui faciliterait l’attachement). Cette petite étude fragile de Swaab ne nous avance pas à grand chose sinon à la supposition que l’équipe n’a pas trouvé de différence de volume du noyau lui-même, car elle l’aurait très certainement signalé sinon.
Bref, il n’y a vraiment rien qui permette de dire que le noyau paraventriculaire de l’hypothalamus est plus volumineux « chez l’homme » ou « chez la femme », et j’espère donc que Jacques Balthazart ne le prétend pas.
Le noyau ventromédian de l’hypothalamus (VMN ou WMH)
Situé au sein d’une région notamment impliquée dans la régulation de la prise alimentaire, le noyau ventromédian de l’hypothalamus semble chez les rongeurs participer à des mécanismes déclenchés par la perception de phéromones via l’organe voméronasal, et jouer en particulier un rôle clé dans la manifestation d’un aspect central du comportement sexuel typique des femelles chez les rongeurs (également manifesté par les mâles, mais de manière plus sporadique), le réflexe de lordose.
Ce réflexe qui chez la rate, après amorçage par la présence d’un certain niveau d’œstradiol puis de progestérone (œstrus), est déclenché par des stimuli typiquement fournis par ses congénères mâles, est l’un des mécanismes « sélectionnés pendant 3,5 milliards d’années » qui a inexplicablement « subitement » disparu uniquement chez nous et nos plus proches cousins. Il semble en effet que ni la perception de fragrances masculines, ni « les stimulations sexuelles sur la croupe de la femme ne déclenchent plus la position de lordose », et que « quand une femme se met à quatre pattes, courbe son dos et reste immobile, ce n’est plus un mouvement réflexe déclenché par un stimulus sexuel, mais un mouvement volontaire », pour reprendre le vocabulaire poétique de feu Serge Wunsch.
De même, comme le souligne un tout récent éditorial publié dans Science, aucune phéromone humaine n’a jamais pu être mise en évidence[12], que ce soit la « copuline » censée se trouver dans les sécrétions vaginales surtout autour de l’ovulation et déclencher l’augmentation chez les hommes de « la testostérone, hormone du désir », selon Science et Vie en 1996[13], Pierre Bustany dans La biochimie du coup de foudre en 1997[14] ou encore René Zayan dans Du baiser au bébé en 2005[15], l’androstenone censée inconsciemment attirer les femmes et repousser les hommes selon Pierre Bustany[16] ou encore René Zayan[17], ou bien la mystérieuse phéromone censée provoquer la synchronisation des cycles menstruels des femmes vivant ensemble, un mythe savant persistant né d’une petite étude mal faite publiée en 1971 (et amplement reformulée dans la vulgarisation) alors que ce phénomène de synchronisation est manifestement inexistant[18].
Dans Biologie de l’homosexualité, Jacques Balthazart évoque le noyau ventromédian de l’hypothalamus en expliquant que symétriquement à la partie médiane de l’aire préoptique pour le « comportement sexuel mâle », ce noyau est le site d’action des stéroïdes « nécessaire et suffisant » pour activer le « comportement sexuel femelle » (p. 70). Il pose dans un premier temps qu’il est plus volumineux « chez les rats femelles que chez les mâles » (p. 80), finissant par écrire que « dans la foulée de l’identification [du] SDN dans l’aire préoptique chez de nombreuses espèces, les anatomistes ont […] identifié diverses structures qui sont soit plus volumineuses chez les mâles que chez les femelles (noyau de la strie terminale du rat) soit chez les femelles que chez les mâles (noyau ventro-médian de l’hypothalamus) » (p. 84, souligné par moi). La mention des « nombreuses espèces » et la suppression de « du rat » peut laisser croire qu’une différence F>M de volume du noyau ventromédian est établie entre autres aussi dans notre espèce, d’autant que Jacques Balthazart ajoute ici qu’il reviendra sur ce sujet dans le chapitre consacré à l’analyse détaillée des « différences morphologiques entre cerveau [sic] des hommes et des femmes » (p. 84). Il ne fournit cependant nulle part dans le livre d’information concernant une éventuelle différence femmes-hommes de volume de ce noyau, et pour cause.
En 2013, Chung et Auger écrivaient que la région ventromédiane de l’hypothalamus était chez le rat plus volumineuse chez le mâle que chez la femelle et qu’on ne savait pas si cette région présentait un dimorphisme de volume chez l’être humain. J’ai pour ma part cherché en vain des données indiquant un éventuel dimorphisme de volume de cette région ou ce noyau chez l’être l’humain.
J’ai bien trouvé une étude à nouveau faite par le groupe de Dick Swaab, mais elle ne conforte ni les écrits, ni les sous-entendus de Jacques Balthazart. Ishunina et al. 2001 commencent par signaler que si ce noyau a été trouvé plus volumineux chez la femelle dans une espèce de lézard, chez le rat il a au contraire été trouvé plus volumineux chez le mâle, les noyaux des cellules de ce noyau ayant selon ell∙eux été trouvés plus volumineux chez les rates que chez les rats. Il semble que Jacques Balthazart a lu un peu trop vite… La différence dans le sens M>F chez le rat est pourtant clairement affirmée et documentée dans l’ouvrage dirigé par Ivanka Savic qui fait référence chez les adeptes de ses croyances[19], mais il était manifestement trop désireux de voir chez le rat un résultat flattant la logique simpliste qui sous-tend son interprétation des différences de volumes.
Au vu des études publiées par Swaab sur d’autres noyaux, étant donné qu’il connaissait l’existence de dimorphismes du volume de ce noyau dans au moins deux espèces et sachant qu’il avait à sa disposition les échantillons nécessaires pour faire la comparaison chez des humains, on peut raisonnablement penser que s’il n’a rapporté aucun constat de différence significative ni dans Ishunina et al. 2001, ni ailleurs, c’est qu’il n’a pas trouvé de différence de volume entre femmes et hommes dans le noyau ventromédian de l’hypothalamus.
Dans cette étude publiée en 2001, l’équipe dirigée par Swaab s’est penchée sur la taille des cellules nerveuses et celle de leur appareil de Golgi, considérant qu’il s’agissait d’indicateurs de leur activité métabolique. Après analyse des données de son échantillon de coupes histologiques de cerveaux de 28 personnes décédées entre 24 et 94 ans (12 hommes et 16 femmes), elle a fini par (arriver à) trouver et mettre en avant la différence suivante : la taille de l’appareil de Golgi relativement à celle des cellules nerveuses était en moyenne 34 % plus grande chez les femmes que chez les hommes avant 50 ans, et 15 % plus grande chez les hommes que chez les femmes après 50 ans. Pour Swaab et ses collègues, ces résultats (non répliqués) combinés à d’autres données « suggèrent que les androgènes ont un effet inhibiteur sur l’activité des neurones du noyau ventromédian humain », même si « la possibilité que les œstrogènes stimulent l’activité des neurones du noyau ventromédian devrait également être envisagée ». Sans commentaire.
Des études faites par Ivanka Savic concernant des phéromones putatives méritent aussi d’être mentionnées ici bien que n’ayant pas porté sur le volume de ce noyau, car elles concernent cette région de l’hypothalamus et sont citées dans le précédent livre de Jacques Balthazart. Elles ont également été instrumentalisées dans Homo ou hétéro, est-ce un choix ?, un documentaire affligeant de plus (dont j’avais dit deux mots ici) diffusé par France 2 en 2015, pour lequel Jacques Balthazart a fait office de conseiller scientifique aux côtés de René Zayan et Philippe Brenot, et dans lequel l’existence de phéromones humaines était affirmée sans ambages[20].
Il s’agit tout d’abord de Savic et al. 2001, article introduit par la citation d’une poignée de petites études non répliquées voir contredites en faisant comme si leurs résultats étaient acquis, notamment l’étude de 1971 sur la « synchronie menstruelle ». Dans cette étude, l’équipe de Savic a utilisé deux « substances ressemblant à des hormones sexuelles », l’une appelée androstadienone (AND), habituellement trouvée en beaucoup plus grande quantité sous les aisselles des hommes que sous celles des femmes (que des bactéries logeant sur la peau transforment en androstenone, un composé volatile fortement odorant), l’autre appelée estratetraenol (EST), une substance dérivée de l’androstadienone qui n’a été trouvée que dans l’urine des femmes enceintes. L’équipe a mesuré par TEP l’activité cérébrale de 12 femmes et 12 hommes hétérosexuel∙les pendant qu’on leur faisait sentir l’une ou l’autre de ces deux substances, et a trouvé qu’en moyenne, chez les femmes sentir l’AND activait davantage une région de l’hypothalamus incluant l’aire préoptique et le noyau ventromédian que sentir l’EST, alors que chez les hommes, sentir l’AND n’activait presque pas l’hypothalamus et sentir l’EST l’activait davantage, ni plus ni moins que les femmes mais surtout dans une région incluant le noyau paraventriculaire et le noyau dorsomédian. Cette étude jamais répliquée est parfois présentée comme suggérant que le noyau ventromédian pourrait être le lieu d’une « intégration sexuellement dimorphique d’un signal phéromonal » (Chung et Auger 2013), mais cette supposition relève d’une extrapolation faite sur des bases très fragiles. Surtout, ces deux substances sont odorantes, comme cela est bien précisé dans l’article qui précise aussi que 3 sujets initialement recrutés ont été exclus car ils n’arrivaient pas à détecter l’odeur de l’une ou l’autre. Dès lors, toute différence d’activation pourrait très bien s’expliquer par une sensibilité différente à certaines odeurs acquise au fil du vécu (en particulier sexuel) différent des femmes et hommes testés.
Dans Savic et al. 2005, la même équipe a refait le test sur 36 sujets dont la capacité à sentir l’EST et l’AND avait été vérifiée : 12 hommes hétérosexuels, 12 femmes hétérosexuelles, et 12 hommes homosexuels. Elle rapporte qu’en moyenne, sentir l’AND induisait chez ces derniers « une activation ressemblant davantage à celle des femmes hétérosexuelles qu’à celle des hommes hétérosexuels », en particulier dans la région incluant l’aire préoptique et le noyau ventromédian. Comme l’équipe l’admet dans l’article (bien qu’elle privilégie une autre interprétation), ce résultat « pourrait refléter une sensibilisation de l’hypothalamus ou de circuits connexes à l’AND causée par une exposition répétée à des contacts sexuels avec des hommes », et une autre possibilité serait que « les femmes hétérosexuelles et les hommes homosexuels ont associé l’AND à la sexualité, tandis que les hommes hétérosexuels ont fait une association similaire avec l’EST ». L’étude de Berglund et al. 2006 dirigée par Savic rapporte les résultats de la même comparaison faite cette fois avec 12 femmes homosexuelles. L’équipe rapporte que l’activation chez elles a en moyenne différé de celles des 12 femmes hétérosexuelles, mais ce uniquement pour l’AND, et ce uniquement dans l’aire préoptique (non activée chez les premières au contraire des secondes), alors que l’EST avait montré une tendance similaire à celle des hommes hétérosexuels (mais non significative) à activer le noyau dorsomédian. Cette étude qui comme les précédentes, n’a pas fait l’objet d’une réplication indépendante n’apporte donc rien de plus sur le noyau ventromédian, et ne fait que suggérer que la réaction des femmes homosexuelles à certaines odeurs corporelles sexuées est plus proche de celle des hommes hétérosexuels que de celle des femmes hétérosexuelles.
Bref, contrairement à ce que peuvent laisser penser les insinuations de Jacques Balthazart, appuyées en outre par une fausse information concernant le rat, rien ne permet de dire que le noyau ventromédian de l’hypothalamus est plus volumineux « chez la femme » ni que sa taille joue un rôle dans la sexuation du comportement sexuel humain.
Le noyau arqué ou infundibulaire de l’hypothalamus (INF ou arcuate nucleus)
Le noyau arqué ou infundibulaire de l’hypothalamus est un centre important de régulation de l’homéostase (il est impliqué dans le contrôle de la prise alimentaire, du métabolisme, de la température du corps), intervenant également dans la régulation cardiovasculaire ou encore la croissance, mais aussi dans la sécrétion de la GnRH, via ses neurones à neurokinine B et ses neurones à kisspeptine (découverts dans les années 2000).
La GnRH, dont le réveil de la production par l’hypothalamus signe le début de la puberté, stimule la sécrétion de LH et de FSH par l’hypophyse, deux hormones qui une fois relâchées dans la circulation générale, agissent sur l’activité des testicules et des ovaires (axe gonadotrope), les hormones produites par les gonades agissant en retour sur le système hypothalamo-hypophysaire en régulant la sécrétion de LH et FSH (rétrocontrôle). Le noyau arqué est donc aussi un bon candidat à la monstration d’un dimorphisme de sexe naturel, et Dick Swaab s’est également penché dessus, cette fois en collaboration avec Julie Bakker.
Ex-membre du laboratoire de Jacques Balthazart à l’Université de Liège, Julie Bakker y dirige depuis 2003 son propre groupe de recherche. Comme indiqué sur sa page du site de l’université, elle « se focalise sur la différenciation sexuelle du cerveau », utilisant pour ce faire des modèles de souris transgénique et des modèles humains, à savoir des « patients souffrant de troubles de la différenciation sexuelle » (page consultée le 18 mai 2019). Je relève à nouveau au passage l’emploi d’un vocabulaire connoté, à mes yeux très révélateur d’une vision binaire normative du sexe et irrespectueux tant de la demande des personnes intersexes d’être désignées sans pathologisation que de la terminologie désormais employée par les spécialistes de leur prise en charge biomédicale : on parle en effet de « personnes avec variations du développement sexuel », et non de « patients souffrant de troubles », a fortiori de troubles « de la différenciation sexuelle ». De manière cohérente avec cette vision, Julie Bakker est à la recherche de déterminants hormonaux de l’« identité sexuelle » – terminologie également signifiante –, conçue comme un tout fait de féminité/masculinité cérébrale incluant l’orientation sexuelle. Cette chercheuse croit en particulier qu’il existe des phéromones dans notre espèce, et qu’hommes et femmes y ont des « réactions instinctives » différentes (voir cette interview faite en 2009).
Suite à la publication de données indiquant que les neurones à neurokinine B et les neurones à kisspeptine de ce noyau étaient impliqués dans la sécrétion de GnRH, l’équipe menée par Julie Bakker s’y est intéressée. Dans la droite ligne des travaux initiés par Gunter Dörner, menés entre 1975 et le début des années 1990 à la recherche d’un lien entre homosexualité ou transidentité et capacité du système hypothalamo-hypophysaire à réagir à une haute dose d’œstrogènes par un pic de LH (voir Jordan-Young 2016 [2010] p.190-194), l’équipe a comparé les volumes de ces neurones entre femmes et hommes, ainsi qu’entre sujets « contrôles » et sujets trans ou homosexuels.
Taziaux et al. (2012) rapporte l’étude des neurones à neurokinine B chez 18 femmes et 18 hommes non trans et 5 personnes trans MtF, décédés entre 5 mois et 90 ans – l’article emploie des expressions telles que « adult men, adult women, and adult MtF transsexuals », faisant des sujets trans des êtres à part n’étant ni des femmes, ni des hommes. L’équipe trouve que le volume occupé par les neurones à neurokinine B du noyau infundibulaire ne diffère pas dans l’enfance et l’adolescence, mais qu’il est à l’âge adulte en moyenne plus grand chez les femmes que chez les hommes, ce « dimorphisme sexuel à dominance féminine » s’accroissant en outre après la ménopause. Elle en déduit que la sécrétion des hormones gonadiques à partir de la puberté pourrait faire émerger une différence entre femmes et hommes inexistante dans l’enfance « en complément de la période prénatale bien connue d’organisation du cerveau dépendante des hormones stéroïdiennes ». Ce résultat n’apporte donc pas d’eau au moulin de la thèse défendue ici par Jacques Balthazart.
L’équipe rapporte aussi que ce volume moyen ne diffère pas entre les femmes et les cinq sujets MtF ayant suivi un traitement hormonal de réassignation. Dans sa discussion des résultats, elle estime que « l’inversion du sexe » observée chez les sujets MtF « pourrait refléter, au moins en partie, une différenciation sexuelle atypique de l’hypothalamus », mais notons à nouveau que cela pourrait tout aussi probablement refléter l’effet du traitement hormonal de réassignation.
Par ailleurs, comme cela est mentionné très vite en passant, l’équipe n’a pas trouvé de différence entre femmes et hommes dans le volume du noyau infundibulaire lui-même, ce qui n’apporte donc pas non plus de soutien à l’affirmation de Jacques Balthazart concernant l’existence de noyaux plus volumineux « chez la femme ».
Dans Taziaux et al. (2016), l’équipe s’est penchée sur les neurones à kisspeptine du noyau infundibulaire. Leur étude a porté sur 61 personnes décédées : 23 femmes et 20 hommes contrôles, 3 hommes hétérosexuels et 5 hommes hétérosexuels séropositifs, 8 personnes trans MtF et 1 FtM ayant suivi un traitement hormonal, et une personne trans MtF sans traitement hormonal. Elle trouve que le nombre de ces neurones tend à suivre une courbe en U au fil du temps (haut dans l’enfance, bas à l’âge adulte puis à nouveau haut chez les personnes âgées), ce qui est « assez inattendu au vu de ce qui a été observé dans les études animales », et ce qui « reflète probablement la fluctuation du taux d’hormones stéroïdiennes [dans le sang] au cours de la vie », leur interprétation des données sur les hommes homosexuels de leur échantillon allant également en ce sens[21]. Elle trouve également que ce nombre est en moyenne supérieur chez les femmes, et qu’il est « typiquement féminin » chez les sujets MtF ayant suivi un traitement à base d’œstrogènes – ce qui là encore suggère un effet des œstrogènes, mais l’équipe préfère à nouveau suggérer que cette « inversion du sexe [sic] pourrait refléter, au moins en partie, une différenciation sexuelle atypique de l’hypothalamus ».
Avant l’équipe de Julie Bakker, Hrabovszky et al. 2010 et Hrabovszky et al. 2011 avaient déjà trouvé un plus gros volume moyen des neurones à kisspeptine et neurokinine B dans le noyau infundibulaire des femmes que dans celui des hommes, les premiers en particulier étant en contact plus étroit avec les neurones à GnRH chez les femmes. Ces chercheur∙es relèvent que leurs résultats convergent avec d’autres ayant indiqué une hypertrophie des neurones à kisspeptine et neurokinine B après la ménopause, et estiment que le noyau infundibulaire est probablement le ou l’un des sites de l’hypothalamus où a lieu le rétrocontrôle négatif de la sécrétion de GnRH, c’est-à-dire la réduction de celle-ci notamment par la progestérone et l’œstradiol à faible dose (c’est sur ce mécanisme que repose l’efficacité contraceptive des composés œstro-progestatifs, ainsi que leur capacité à diminuer l’activité testiculaire dont la production de testostérone chez les personnes trans MtF qui les utilisent à cette fin). Selon cette équipe, du fait de leurs gonades différentes, il existe des différences entre femmes et hommes dans ce noyau en particulier au niveau des neurones à kisspeptine, celles-ci sont nettement accrues par la ménopause, et « il reste à établir si l’exposition différentes aux stéroïdes sexuels durant le développement a une quelconque contribution au dimorphisme sexuel du système à kisspeptine de l’hypothalamus » (Hrabovszky et al. 2011).
Si Jacques Balthazart pensait à ce noyau en évoquant l’existence de noyaux plus volumineux « chez la femme », on pourrait à la rigueur trouver cela correct en appliquant cette idée non pas au noyau lui-même mais à un sous-ensemble des neurones qu’il contient. Cependant, les indices d’un lien avec des comportements humains sont excessivement vagues et fragiles, et rien dans les données disponibles ne plaide en faveur de l’idée que cette différence est créée par un effet de la testostérone périnatale chez les garçons. Il se pourrait après tout que ce noyau impliqué dans le contrôle de l’ovulation ne subisse aucune sexuation périnatale, sachant que chez l’humain et le macaque rhésus au moins, la testostérone périnatale n’empêche pas les mâles adultes de réagir par un pic de LH à une haute dose d’œstradiol comme les femelles, au contraire des rongeurs (voir Vargas-Trujillo et al. 2017) – encore un mécanisme de sexuation d’un phénomène fondamental partagé par tous les mammifères qui a pourtant « disparu subitement ».
Les corps mamillaires de l’hypothalamus
Les corps mamillaires sont des noyaux formant la bordure caudale de l’hypothalamus, au sein desquels on distingue le noyau médial et le noyau latéral. Le noyau médial est connu pour son rôle dans la formation et le rappel des souvenirs autobiographiques. Dans Ishunina et al. 2003, Swaab et ses collaborateur∙ices indiquent que les corps mamillaires font aussi partie d’un circuit participant au contrôle de l’érection, et que des observations ont été faites chez le macaque et l’humain associant la lésion des corps mamillaires à une puberté précoce.
Dans cet article rapportant une étude à nouveau dirigée par Dick Swaab, donc, les auteur∙es écrivent qu’un dimorphisme sexué a été observé chez le rat, citant Lopez et al. 1994 (cette étude menée sur un échantillon de seulement 6 rats Wistar de chaque sexe a trouvé que les noyaux des corps mamillaires étaient en moyenne plus volumineux chez les mâles, environ 1.5 fois d’après les figures, l’information n’étant pas donnée dans le texte), ajoutant qu’un dimorphisme sexué a aussi été observé chez l’humain, citant Sheedy et al. 1999 en référence (ainsi que Raz et al. 1992 n’ayant pas trouvé de différence significative, mais cette étude est de peu de poids face à celle de 1999 car elle n’a porté que sur 82 sujets). Cette affirmation a ensuite été prise pour argent comptant dans d’autres articles sans remonter à sa source, que j’ai quant à moi examinée comme je le fais systématiquement.
Dans cette grosse étude faite sur 2212 cerveaux, dont 2048 jugés avoir des corps mamillaires non pathologiques, Sheedy et collègues ont effectivement trouvé une différence statistiquement très significative parmi ces derniers, mais il est pour le moins osé de la qualifier de dimorphisme. En effet, le volume moyen observé chez les hommes était de 65.3 mm3 +/- 20.0, versus 59.8 mm3 +/-19.2 chez les femmes, ce qui fait un volume environ 9 % plus important en moyenne chez les hommes (ainsi qu’une grande variabilité à l’intérieur de chaque groupe de sexe). Comme les auteur∙es de l’étude le soulignent à la fin de leur article, cette différence est cohérente avec la différence moyenne femmes-hommes de volume total du cerveau.
En d’autres termes, contrairement à ce qu’ont prétendu Dick Swaab et ses collègues, cette grosse étude plaide plutôt pour l’absence de dimorphisme sexué dans le volume de cette structure, au sens où nous l’avons vu plus haut (chapitre II). Le groupe de Swaab n’a pas apporté depuis de résultats susceptibles de contredire cette conclusion, et mes recherches ne m’ont permis d’identifier que la petite étude de Bernstein et al. 2012, qui a certes trouvé une différence moyenne plus nette (68 mm3 versus 49 mm3), mais sur un groupe contrôle composé de seulement 8 hommes et 12 femmes.
Par ailleurs, je signale que Swaab a également publié une étude mettant la densité des récepteurs aux androgènes dans les corps mamillaires en lien avec « le niveau d’androgènes en circulation, mais pas l’orientation sexuelle ni l’identité de genre » (Kruijver et al. 2001).
En bref, les données disponibles sur les corps mamillaires n’indiquent pas l’existence d’une différence de volume susceptible de conforter le propos de Jacques Balthazart, et d’autres différences observées dans ces noyaux sont à mettre en relation avec la physiologie de la reproduction proprement dite plutôt qu’avec des comportements.
En synthèse sur les noyaux humains présumés « sexuellement différenciés » visibles uniquement dans des coupes histologiques
En synthèse, nous avons vu que Jacques Balthazart a tenu par le passé un discours plus que fallacieux sur certains noyaux, qu’il se livre encore une fois dans cette interview à une présentation trompeuse de certains résultats de la recherche, et que celle-ci n’a pas démontré l’existence d’une « bonne dizaine » de noyaux visibles uniquement dans des coupes histologiques dont il serait établi que le volume diffère entre femmes et hommes, dans le cerveau tout au moins (le discours de Jacques Balthazart étant centré sur celui-ci et ce texte étant déjà très long, je n’ai pas abordé la question de la sexuation de noyaux du système nerveux central situés en dehors du cerveau, dont le noyau bulbocaverneux de la moelle épinière ou noyau spinal d’Onuf chez l’humain, qui contrôle des muscles du périnée impliqués dans l’érection du pénis et du clitoris ; il y aurait beaucoup à dire sur ce noyau en particulier, qui n’est pas sexué chez le rat par le même mécanisme que le SDN-POA et qui présente chez l’être humain un dimorphisme bien moins marqué).
De plus, les données disponibles sur les rares noyaux pour lesquels une différence moyenne de volume entre femmes et hommes a été mise en évidence, ou est au moins indiquée par de petites études non répliquées, ne montrent jamais de dimorphisme tel qu’ils pourraient être dits plus volumineux « chez l’homme » ou « chez la femme ».
Par ailleurs, l’éventuelle influence de la testostérone périnatale sur le volume de ces noyaux chez les hommes (et par suite la détermination d’une différence entre femmes et hommes, selon la théorie promue par Jacques Balthazart) reste à démontrer, et les données disponibles plaident parfois plutôt contre l’idée qu’elle est notable le cas échéant. Compte tenu de la participation de ces noyaux à des circuits cérébraux activés dans divers contextes tels que l’activité physiologique des gonades, le fait d’avoir une activité sexuelle ou encore la soumission à un stress, le vécu en moyenne différent des femmes et des hommes est susceptible de créer certaines différences moyennes dans ces noyaux.
Enfin, aucun corrélat comportemental ne peut à ce jour être considéré comme établi avec la taille de ces noyaux chez l’être humain, ni a fortiori un lien de causalité entre elle et des différences comportementales entre femmes et hommes. En revanche, du fait de l’implication de certains noyaux dans la régulation de la physiologie de la reproduction proprement dite, il n’est ou serait pas étonnant qu’ils puissent présenter un certain degré de sexuation périnatale du fait du dimorphisme des appareils génitaux féminin et masculin.
(à suivre)
Odile Fillod
__________________
Notes
[1] Voir dans l’introduction de Biologie de l’homosexualité, p.13 (souligné pour mettre en évidence le caractère tautologique de ce discours) : « Les études animales sont ici d’un grand support. Elles démontrent en effet l’existence chez l’animal de mécanismes neurobiologiques déterminant le comportement et l’orientation sexuelle qui se retrouvent mutatis mutandis dans l’espèce humaine. Ces travaux expérimentaux, réalisés dans des conditions hautement contrôlées, apportent donc des arguments de poids pour interpréter les études largement corrélatives réalisées chez l’Homme. » L’usage que fait Jacques Balthazart de l’expression « mutatis mutandis » me paraît bien décrit par cette définition trouvée en ligne : « Expression latine utilisée commodément dans le cadre d’une comparaison entre des situations que l’auteur entend présenter comme étant similaires. Il ne retient que ce qu’elles ont en commun, écartant les différences et l’expression — littéralement en changeant ce qui doit être changé — lui évite de décrire ces dernières. »
[2] Article intitulé “A review of the status of brain structure research in transsexualism”. Une lecture trop rapide de la Table 11 de cet article peut donner l’impression qu’une « bonne dizaine » de structures présentant un dimorphisme sexué ont été identifiées chez l’être humain. Cette revue de la littérature souffre par ailleurs de certains biais courants dans la littérature de ce champ d’études. En particulier, dans cet article qui passe en revue de nombreuses différences neuroanatomiques « normatives » entre les sexes (afin de mettre en regard des comparaisons entre personnes trans et non-trans), la question cruciale des modalités d’ajustement au volume total du cerveau ou au volume intracrânien (voir le chapitre II de la partie 1) n’est pas du tout adressée correctement.
[3] Je précise que la liste des références citées dans ce qui suit englobe et dépasse celle citée par Guillamon et al. (2016) au titre de la documentation des différences de volumes entre femmes et hommes, et a fortiori celle donnée fin 2018 par Dick Swaab, le grand spécialiste et principal contributeur à l’étude de ces fameux noyaux chez l’être humain, à l’appui de l’idée que de nombreux « dimorphismes sexuels » ont été repérés dans le cerveau humain : « Since the pioneering studies showing that sexual behavior is shaped by the effect of hormones on the brain during early development (Phoenix, Goy, Gerall, & Young, 1959) [NB : étude portant sur un aspect du comportement sexuel mâle menée sur des cochons d’Inde], a great body of research has been performed to explain the complex mechanisms underlying sexual behavior (for a review see McCarthy, 2016). This line of research led to the detection of sexual dimorphism in a number of brain areas during the past 40 years in the rat (Gorski, Gordon, Shryne, & Southam, 1978), guinea pig (Bleier, Byne, & Siggelkow, 1982; Hines, Davis, Coquelin, Goy, & Gorski, 1985), hamster (Greenough, Carter, Steerman, & DeVoogd, 1977), pig (van Eerdenburg, Poot, Molenaar, van Leeuwen, & Swaab, 1990), and human (Allen, Hines, Shryne, & Gorski, 1989; Swaab & Fliers, 1985; Zhou, Hofman, Gooren, & Swaab, 1995; Zhou, Hofman, & Swaab, 1995b) » (Graïc et al. 2018, souligné par moi).
[4] Swaab a publié une seconde observation de différence statistiquement significative de volume de ce noyau (qu’il appelle désormais intermediate nucleus, abrégé InM) en 2011 avec sa collaboratrice Alicia Garcia-Falgueras, à nouveau sur un petit échantillon de convenance, lorsque n’étaient pris en compte que les 13 hommes et 12 femmes décédés entre 10 et 45 ans de celui-ci (Garcia-Falgueras et al. 2011). Il ne s’agit pas d’une réplication indépendante puisque c’est à nouveau le labo de Swaab qui a fait cette étude.
[5] Il est depuis quelques années parfois aussi appelé « noyau périventral » ou « subdivision latérale du noyau unciné », lorsqu’on appelle noyau unciné (uncinate nucleus) la réunion des INAH 3 et 4.
[6] Après la publication de son article de 1991, qui a fait l’effet d’une véritable bombe médiatique, LeVay a quitté son poste d’enseignant chercheur. Homosexuel militant, il a depuis abandonné toute recherche en biologie pour se consacrer par d’autres moyens à la défense de l’idée que l’orientation sexuelle est fortement influencée par des facteurs biologiques innés. Ses uniques publications dans une revue scientifique depuis 1991 sont d’une part l’introduction du numéro spécial de Frontiers in Neuroendocrinology d’avril 2011 consacré à la « différenciation sexuelle du comportement sexuel et de son orientation », tribune donnée aux principaux chercheurs ayant voué leur carrière à la tentative de mise en évidence de tels facteurs biologiques, et d’autre part un commentaire sur Breedlove (2017) dans Archives of Sexual Behavior.
[7] Voir dans Jean-François Marmion, juillet 2010, « Tu l’aimes, mon hypothalamus ? », Sciences Humaines, n°217, p.40-42 (Dossier « Les secrets de la séduction »), article basé essentiellement sur les écrits du docteur en neurosciences et journaliste spécialisé Sébastien Bohler : « Dans les vingt secondes suivant la rencontre d’une jolie inconnue, la production de deux hormones de ces messieurs, la testostérone et le cortisol, liées respectivement au désir sexuel et à la motivation, fait un bond. […] Ces hormones sont produites par l’hypothalamus [pas du tout !!], au centre du cerveau. Sa région plus spécifiquement dévolue aux comportements d’approche sexuelle est deux fois plus importante chez l’homme que chez la femme ». Dans Quand vos gestes parlent pour vous (2012, Dunod), Sébastien Bohler précise : « Les hormones androgènes […] sont libérées par les testicules, pénètrent dans le cerveau et y sont transformées en œstrogènes par une enzyme appelée aromatase. L’action des œstrogènes ainsi produites chez l’embryon conduit à ce qu’on appelle une masculinisation du cerveau, qui comprend notamment le développement d’une zone de l’hypothalamus responsable des comportements d’approche sexuelle » (p.122). Pour d’autres exemples des méfaits de Sébastien Bohler, voir les cinq articles dans lesquels je le mentionne, dont ceux de décembre 2012 et janvier 2013 qui lui sont exclusivement consacrés.
[8] Cf dans GORSKI Roger A. (2000) « Sexual differentiation of the nervous system », in Kandel, Schwartz et Jessel (Dirs), Principles of Neural Science, 4è. Éd, Ed. Appleton and Lange, p. 1131-1149 : « Genetic males with the androgen insensitivity syndrome (Table 57-1) are psychosexually female. These ‘women’ develop feminine phenotypes at puberty because of their testicular activity and the aromatization of testosterone. Their feminine psychosexuality is seemingly in accord with the idea that the developmental default state of sexual differentiation is female. However, this interpretation is at odds with the general view that estrogen is actually the masculinizing hormone in sexual differentiation of the brain. Perhaps humans have some protective mechanism, akin to α-fetoprotein, that protects the developing brain from exposure to estrogen, or perhaps estrogen is not the masculinizing hormone in humans. »
[9] Par exemple, Jeong et al. (2008) documentent une manipulation hormonale périnatale ayant empêché le développement normal de ce noyau chez des rats mâles, et relèvent que cette manipulation a réduit la taille du SDN-POA à l’âge adulte et « certaines composantes du comportement sexuel mâle telles que la monte et l’intromission, mais pas la préférence de partenaire sexuel ». Le groupe de Dick Swaab a quant à lui documenté dans Olvera-Hernandez et al. 2017 une expérience de blocage périnatal de l’aromatase chez des rats mâles ayant abouti en moyenne d’une part à une modification de la « préférence de partenaire », et d’autre part à une réduction du volume et du nombre de neurones du SDN-POA (ainsi que du noyau suprachiasmatique), mais a trouvé que ces deux phénomènes étaient indépendants (i.e. le volume était réduit « indépendamment de la préférence de partenaire »). En fait, les données que Jacques Balthazart mobilise concernant le SDN-POA du rat portent essentiellement sur les comportements de monte/intromission, indépendamment du sexe du congénère monté (ou par lequel un rat mâle peut se laisser monter), plutôt que sur des aspects pouvant ressembler davantage (quoique de loin) à la notion humaine d’orientation sexuelle. Comme l’a souligné Rebecca Jordan-Young 2016 [2010], ce « raisonnement basé sur l’équivalence entre comportements sexuels typiques des mâles (notamment la monte) et orientation sexuelle typique des mâles a fait l’objet de critiques dévastatrices », dont en 1985 par Anne Fausto-Sterling et en 1993 par William Byne, l’auteur de la (non-)réplication partielle de Levay 1991 (p. 289-290). Allant dans le même sens, Ngun et Vilain (2014) soulignaient plus récemment : « it is true that manipulation of prenatal and/or perinatal hormonal levels in rodents has been shown to lead to changes in mating/sexual behavior […] However, changing sex-stereotyped mating behavior is not the same as changing the sexual orientation or partner preference of that animal. Inducing lordosis in a male does not make it prefer males over females. It will accept mounts from females as well. ».
[10] En 1984 déjà, Gorski et Arnold soulignaient que sachant que chez le furet, le volume de ce qui semblait être l’équivalent du SDN-POA du rat était modifié par les hormones à l’âge adulte, il était peut-être prématuré de penser que chez le rat, celles-ci étaient sans effets. Des études ultérieures ont trouvé que la taille du SDN-POA et la préférence de partenaire pouvaient être modifiés par l’expérience sexuelle et les hormones en circulation (voir par exemple Bloch et Gorki 1984 et Woodson et al. 2002 par le groupe de Gorski et Xiao et al. 2004 par un labo japonais). Des recherches menées chez le rat depuis les années 2000 par le chercheur canadien James Pfaus et un groupe de chercheurs mexicains dirigé par Genaro Coria-Avila indiquent aussi qu’il est possible d’agir sur les préférences sexuelles des rats mâles et femelles à l’âge adulte. En particulier, ces chercheur∙es ont montré qu’on pouvait augmenter la préférence pour les mâles chez des rats mâles adultes n’ayant pas encore eu d’expérience sexuelle avec une femelle. Il suffisait pour cela de les faire cohabiter avec un mâle sexuellement expérimenté tout en leur administrant soit une molécule activant certains récepteurs de la dopamine, soit une molécule activant les récepteurs de l’ocytocine. Après arrêt du traitement, ces mâles présentaient en moyenne non seulement un comportement homo-social plus marqué que les mâles non conditionnés (ils s’approchaient plus volontiers d’un mâle, passaient plus de temps avec lui, engageaient plus rapidement un contact physique et passaient plus de temps contre lui, reniflaient davantage son corps et ses parties génitales), mais aussi des signaux d’attirance pour les mâles plus marqués : en moyenne, par rapport à des mâles non conditionnés, ils sollicitaient davantage un mâle à la manière typique dont les femelles sollicitent sexuellement, et présentaient davantage d’érections induites par la présence du mâle. En outre, ces modifications comportementales n’étaient pas associées à une modification du volume du SDN-POA (Triana-Del Rio et al. 2015).
[11] Cf dans Bakker et al. 2006 : « The classic view of sexual differentiation in mammalian species is that testosterone secreted by the testes causes masculinization (increase in male-typical characteristics) and defeminization (decrease in female-typical characteristics) of the brain and behavior. Many of these actions of testosterone on the developing brain are mediated by estradiol, which is formed locally in the brain through the transformation of testosterone by the enzyme aromatase (the ‘aromatization hypothesis’; refs. 6-8). […] Our results show that the principal action of prenatal estrogen exposure, regardless of whether it occurs in female or male mice, is to defeminize and, to some extent, masculinize brain and behavior; further, we show that AFP [Alpha-fetoprotein], which binds estradiol circulating in the female fetus with high affinity and capacity, protects the developing brain from a male-typical organization by this steroid. […] It is unclear whether, in other species, AFP similarly protects the brain from estrogens during sexual differentiation. In contrast to AFP in mice and rats, human AFP does not bind estrogens, although, notably, AFP has been reported to have an antiestrogenic activity in estrogen-sensitive breast cancers, probably by a mechanism other than the sequestration of estrogen. In primates, the main high-affinity steroid hormone–binding protein (androgens and to a lesser extent estrogens) is the sex hormone–binding globulin (SHBG), which has little structural homology with AFP. The primate SHBG may have a function in embryonic development similar to that of AFP in rodent species. It should be noted that androgen is the main hormone causing brain masculinization in primate species[*]. SHBG may thus protect the developing female human brain from being masculinized by androgens. » [*] : les auteur∙es citent ici en référence Wallen 2005, qui défend l’idée que l’aromatisation n’intervient pas ou peu dans la sexuation pré- ou périnatale des comportements des primates non humains.
[12] Kai Kupferschmidt, 12/04/2019, « Atmospheric scientists join pheromone quest », Science vol. 364(6436), p. 112. Extrait : « Since 1959, when German biochemist Adolf Butenandt isolated the first pheromone—a compound named bombykol that female silkmoths use to attract partners—generations of researchers have looked for similarly powerful chemicals in humans. But they haven’t identified a single one. The few high-profile claims, for example that women living together synchronize their menstrual cycle through chemical signals, have not stood the test of time. “The field is in a bit of a crisis,” says Andreas Natsch, a researcher at the fragrance company Givaudan in Vernier, Switzerland. »
[13] Roman Ikonicoff, « Parfum de femme », Science & Vie n°950, nov. 1996, p.16, rubrique « Actualité – Recherche » : « Il semble que l’homme est sensible à l’ovulation de la femme. Astrid Jutte, du laboratoire d’éthologie urbaine de l’institut Ludwig-Boltzmann, à Vienne (Autriche), vient d’en apporter la preuve grâce à une étude statistique menée sur 106 hommes. Elle a constitué quatre groupes d’hommes, auxquels elle a fait humer une vapeur différente, trois contenaient des acides gras (fabriqués synthétiquement pour l’expérience) qu’on trouve dans le vagin des femmes : la copuline. La quatrième ne contenait que de la vapeur d’eau. La copuline de la première solution correspondait à la période d’ovulation ; celle de la deuxième, à la menstruation; celle de la troisième à un moment quelconque du cycle. Après avoir fait sentir les vapeurs à ses sujets, Astrid Jutte mesura le taux de testostérone – l’hormone sexuelle masculine – contenue dans leur salive. Le taux le plus élevé se trouvait dans le groupe qui avait humé la “vapeur de l’ovulation”… De quoi donner des idées aux parfumeurs. » Remarques : cette brève est une mauvaise traduction un peu adaptée d’une brève du magazine New Scientist, dont la source était une communication faite en août 1996 au colloque de l’International Society for Human Ethology. Cette étude particulièrement appréciée par certains psychologues évolutionnistes, mais jamais répliquée, n’a donné lieu qu’à un article publié dans une obscure revue de gynécologie en langue allemande : Grammer K., Jütte A. (1997) The war of odours: Importance of pheromones for human reproduction, GYNAKOLOGISCH-GEBURTSHILFLICHE RUNDSCHAU, vol. 37(3), p.150-153. Dans un article publié en 2003 dans Behavioral Ecology and Sociobiology (favorable à ce genre de théories), qui passait en revue les données disponibles relatives aux phéromones putatives chez l’humain, l’absence de données scientifiques étayant cette théorie était soulignée. Il était aussi précisé que selon une étude publiée en 1975 et répliquée en 1981, on trouve dans les fluides vaginaux cinq « copulines » outre l’acide acétique, mais ce chez seulement environ un tiers des femmes, que l’étude de 1981 n’avait pas retrouvé que leur quantité variait selon la phase du cycle menstruel, et que l’auteur de l’étude de 1975 avait déposé en 1972 un brevet en France pour l’utilisation des « copulines »en parfumerie, ce puissant philtre censé provoquer le désir masculin n’ayant semble-t-il finalement pas été commercialisé.
[14] Ce documentaire de Thierry Nolin a été important pour la diffusion dans la culture commune francophone de certains mythes savants aujourd’hui très répandus sur des différences entre les sexes censément innées dans le comportement sexuel. Multi-diffusé sur Arte puis France 5 entre 1997 et 2006, il a aussi été diffusé dans des muséums d’histoire naturelle (au minimum celui de Paris en 2000 et celui de Nancy en 2009). Jean-Didier Vincent, Boris Cyrulnik, Claude Aron et Mireille Bonierbale interviennent également dans ce documentaire. Pierre Bustany est un vieux comparse de Boris Cyrulnik, qui l’emploie comme enseignant dans ses Instituts petite enfance. Sur la « copuline », censée se trouver « chez la femme, dans des sécrétions vaginales d’origine sexuelle » Pierre Bustany explique qu’elle fait partie des phéromones « qui ont été niées jusqu’à ces dernières années », alors qu’elles « agissent comme chez les autres animaux par le biais d’un organe odoriférant qui se trouve dans le nez, le nom savant est organe voméronasal » : « Le rôle des phéromones est évident. Tout au long de l’évolution animale, ces phéromones ont été mises en place pour favoriser un comportement copulatoire au moment où il avait le plus de chances d’être effectif, c’est-à-dire vers le 14ème jour du cycle chez la femme, par exemple. La perception chez l’homme de phéromones féminines peut, petit exemple, déclencher une forte sécrétion de testostérone, ce qui à son tour va rendre l’homme plus entreprenant vers la femelle [sic] ».
[15] Documentaire de Thierry Berrod farci de pseudo-science et d’images trompeuses, produit et diffusé par France 2 puis coédité avec Le Nouvel Observateur en DVD, malheureusement très populaire chez les enseignant∙es de SVT. Extrait des propos de René Zayan : « Le professeur Astrid Jütte, du Boltzmann Institute, a synthétisé une substance odorante produite par les sécrétions vaginales de la femme, la copuline. Résultat : tous les hommes qui ont respiré la copuline trouvent les femmes plus attirantes, même les moins belles. La fonction de la copuline serait donc d’attirer un maximum d’hommes vers les femmes, pour qu’elles choisissent le meilleur. La copuline a également fait augmenter le taux de testostérone, donc la réceptivité sexuelle des hommes. »
[16] Pierre Bustany dans La biochimie du coup de foudre (1997) : « Les phéromones sont très typées suivant les sexes et jouent bien-sûr un rôle d’attracteur pour le sexe opposé et un rôle répulsif pour le même sexe. Les expériences de ces rôles attractif ou répulsif des phéromones sont très nettes : parmi les plus célèbres, c’est le groupe de Klin et Smith à Birmingham University, qui ont concerné plus de 1000 personnes, et ils ont pris un premier groupe de 840 femmes à qui ils ont demandé d’aller s’asseoir dans une salle d’attente dont une des chaises était parfumée, mais à un seuil infra-sensoriel, avec une phéromone masculine. Sur les 840 femmes, 810 femmes se sont assises sur la chaise même, et une dizaine d’autres sur les deux chaises latérales. Quand on fait la même chose (…) mais qu’on fait rentrer un groupe de 540 sujets masculins, tous ont évité soigneusement cette chaise et les deux chaises latérales. On commence actuellement à utiliser commercialement ces dérivés phéromonaux, en particulier l’androstenone. Son dérivé commercial, le Galaxolide, et plus récemment un de ses métabolites actifs, l’Exaltolide, quel joli nom, est utilisé dans des rouges à lèvre à mettre chez les femmes sur la lèvre supérieure dans le but de régulariser les variations de longueur des cycles. » Remarques : l’Exaltolide ou pentadecanolide est un composé odorant utilisé en parfumerie depuis la seconde moitié du 20ème siècle pour son odeur qui rappelle le musc naturel, et n’est pas un métabolite de l’androstenone. Le Galaxolide est également un musc synthétique utilisé comme fragrance, et il est de formule chimique très différente de celle de l’androstenone. Le « groupe de Klin et Smith » n’existe pas, et l’expérience citée par Bustany, réalisée en 1975 par Kirk-Smith et Booth a été racontée dans un colloque sur l’olfaction et le goût dont les actes ont été publiés, mais n’a jamais fait l’objet d’une publication scientifique (confirmé par Kirk-Smith, en 2008). Kirk-Smith et Booth ont publié en 1978 une étude censée montrer que l’inhalation d’androsténol par les femmes augmente la note d’attractivité sexuelle attribuée aux hommes qu’elles voient (Kirk-Smith, Booth, Carroll et Davies, 1978, Human social attitudes affected by androstenol, Research Communication in Psychology, Psychiatry, and Behavior, vol.3(4),p 379-384), qui a été contredite en 1981, et a ensuite tenté de trouver des débouchés de sa « découverte » dans le domaine du marketing (quittant le département de psychologie de l’université de Birmigham, il a d’ailleurs été dans les années 1990 chargé de cours au sein du département Marketing de l’université d’Ulster en Irelande du Nord).
[17] René Zayan dans Du baiser au bébé (2005) : « La testostérone des hommes se transforme en une substance chimique, l’androstérone, que la transpiration véhicule à la surface de la peau. Cette substance sera mangée par de minuscules bactéries qui émettront une odeur plus ou moins agréable. Dans ces vapeurs se trouvent des phéromones inodores. Ces phéromones sont captées par notre organe voméronasal, une petite poche placée dans la paroi du nez. Cet organe primitif n’a en fait aucun rapport avec notre odorat : il envoie directement des signaux à notre cerveau primitif, sans passer par notre cerveau supérieur. Ainsi, nous les percevons inconsciemment pour choisir un partenaire. […] Depuis plus de 40 ans, de nombreux tests ont été effectuées pour révéler l’influence prépondérante des phéromones dans l’attirance sexuelle, même si ces tests sont contestés par une partie de la communauté scientifique. […] Le test des chaises se passe dans une salle d’attente avec environ 12 chaises. L’une d’entre elle a été parfumée d’une phéromone masculine non perceptible. Sur 840 femmes testées, 810 se sont assises sur la chaise masculinisée ou à proximité d’elle. Quand les tests ont porté sur des hommes, ceux-ci l’ont évitée. » Remarques : Il s’agit de la même étude pseudo-scientifique que celle citée par Pierre Bustany (voir la note précédente). La prétendue phéromone censément issue de la décomposition de l’androstérone par des bactéries est l’androstenone.
[18] Plusieurs études ont abouti à la conclusion que le résultat de Martha McClintock, publié en 1971 dans Nature, était un artefact de sa méthodologie (voir notamment Wilson 1992 et Yang et Schank 2006), et même la revue de la littérature de Harris et Vitzthum (2013) pourtant favorable à ce type d’hypothèse conclut à l’absence de preuve empirique de l’existence de ce phénomène (outre que son explication par l’existence de phéromones hypothétique est parfaitement gratuite). Pourtant, Pierre Bustany en parlait en ces termes dans La biochimie du coup de foudre (1997) : « L’effet des phéromones sur les cycles menstruels est extrêmement important. On considère que ces phéromones sont responsables par exemple de la synchronisation des cycles de groupes féminins vivant avec une certaine promiscuité quotidienne ». Je signale que même dans l’étude de McClintock, il n’était pas question de synchronisation des cycles mais de raccourcissement (apparent) de la durée moyenne entre le premier jour des cycles. Michael et Jana 2015 proposent une analyse de la persistance de ce mythe savant en tant qu’exemple de lieu de convergence possible entre féminisme et sociobiologie, qui habituellement s’opposent. Cette convergence se développe actuellement au sein d’un mouvement féministe ou pseudo-féministe sexiste (essentialiste, naturaliste, différencialiste) qui est en France fortement supporté par les argumentaires pseudo-scientifiques de Peggy Sastre, et par ailleurs favorisé par l’essor de l’écoféminisme.
[19] Cf Gagnidze et al. dans Ivanka Savic (dir.), Sex differences in the human brain, their underpinings and implications, Elsevier, 2010, p. 99 : « Notably, the ventromedial nucleus of hypothalamus (VMH), that is critical for the expression of female sexual behavior, is also larger in male than in female rats (Madeira et al., 2001; Matsumoto and Arai, 1983); however, unlike SDN-POA, this difference between the sexes is a result of differences in the volume of neuropils (Madeira et al., 2001) and the number of synapses (Matsumoto and Arai, 1986a,b). » Reférences citées : Madeira, M. D., Ferreira-Silva, L., & Paula-Barbosa, M. M. (2001). Influence of sex and estrus cycle on the sexual dimorphisms of the hypothalamic ventromedial nucleus: stereological evaluation and Golgi study. The Journal of Comparative Neurology, 432, 329–345 ; Matsumoto, A., & Arai, Y. (1983). Sex difference in volume of the ventromedial nucleus of the hypothalamus in the rat. Endocrinologia Japonica, 30, 277–280 ; Matsumoto, A., & Arai, Y. (1986a). Development of sexual dimorphism in synaptic organization in the ventromedial nucleus of the hypothalamus in rats. Neuroscience Letters, 68, 165–168 ; Matsumoto, A., & Arai, Y. (1986b). Male-female difference in synaptic organization of the ventromedial nucleus of the hypothalamus in the rat. Neuroendocrinology, 42, 232–236.
[20] Voix off : « La professeure Ivanka Savic, de l’institut Karolinska de Stockholm, celui-là même où sont décernés les prix Nobels, a fait des découvertes étonnantes en observant la réaction du cerveau à des stimuli. Ivanka Savic soumet à l’IRM fonctionnelle des volontaires homosexuels et hétérosexuels, puis elle compare les résultats. Le cerveau est formé de deux hémisphères, droit et gauche. Dans le groupe hétérosexuel, chez les hommes, les deux hémisphères ne sont pas symétriques, alors que chez les femmes, ils le sont. Dans le groupe homosexuel, c’est l’inverse : chez les hommes ils sont symétriques, et chez les femmes ils sont asymétriques. »
Pr Ivanka Savic, “Neurologue” : « Quand on regarde les sujets homosexuels, les gays sont plus symétriques, comme les femmes hétéros. Et les lesbiennes sont plus asymétriques, comme les hommes hétéros. »
Voix off : « La professeure Savic a aussi mis en évidence des différences significatives dans la perception des phéromones. Ce sont des substances chimiques que chacun de nous émet sans le savoir et qui adressent des messages à l’entourage. ces messages jouent un rôle dans l’attraction sexuelle entre individus. On sait depuis peu que chez l’homme, la perception des phéromones se fait par la muqueuse nasale. »
Pr Ivanka Savic : « Nous avons stimulé le cerveau en laissant le sujet fermer les yeux et respirer calmement. Nous avons présenté les phéromones et les odeurs sous le nez. L’une des phéromones est en fait produite dans la sueur humaine et l’autre est présente dans l’urine de femme. Cette image représente un scan du cerveau de deux groupes de sujets, des gays et des femmes hétérosexuelles. Ils sentent différentes odeurs. Des odeurs ordinaires, des phéromones femelles et des phéromones masculines. Ici c’est une région du cerveau qui est très activée par les phéromones masculines chez les gays, comme chez les femmes hétéros. C’est la région de l’hypothalamus impliquée dans la reproduction. Par contre, quand c’est une phéromone femelle, c’est peu activé chez les gays et les femmes hétéros. Ca active juste les zones normales de l’odorat, ce qui est très différent de la situation précédente. »
Voix off : « D’où vient cette sensibilité particulière aux phéromones ? Est-elle reçue en héritage, ou provient-elle de l’éducation ? En bref, résulte-t-elle de l’inné ou de l’acquis ? »
Pr Ivanka Savic : « Il est très difficile de dire à partir de ces études si ça vient de l’inné, de la naissance, ou de l’acquis. Si nous nous référons uniquement à l’étude anatomique, il est plus difficile d’expliquer ces asymétries par l’apprentissage ou l’expérience. »
Voix off : « Une activation nerveuse peut résulter d’un apprentissage. Avec le temps, par exemple, on devient sensible à l’odeur de transpiration masculine. Mais peut-on changer la symétrie du cerveau, qui reste plastique après la naissance ? La réponse semble être non. »
[21] L’équipe rapporte que le nombre de neurones à kisspeptine du noyau infibulaire ne différait pas en moyenne entre les 3 hommes hétérosexuels séropositifs et les 5 hommes homosexuels séropositifs, notant en revanche qu’il était augmenté chez les premiers par rapport aux hommes hétérosexuels séronégatifs. Elle attribue cet effet à un hypogonadisme causé par le SIDA (l’activité des gonades à l’âge adulte ferait donc bien varier la taille de ce noyau). Dans la discussion des résultats, je note que ces auteur∙es n’hésitent pas à affirmer qu’en revanche, le noyau suprachiasmatique est plus gros chez les hommes homosexuels que chez les hommes hétérosexuels, et que le noyau INAH-3 est au contraire plus petit chez les premiers, ce qui comme on l’a vu est douteux en général et assurément faux pour un nombre conséquent d’hommes homosexuels.

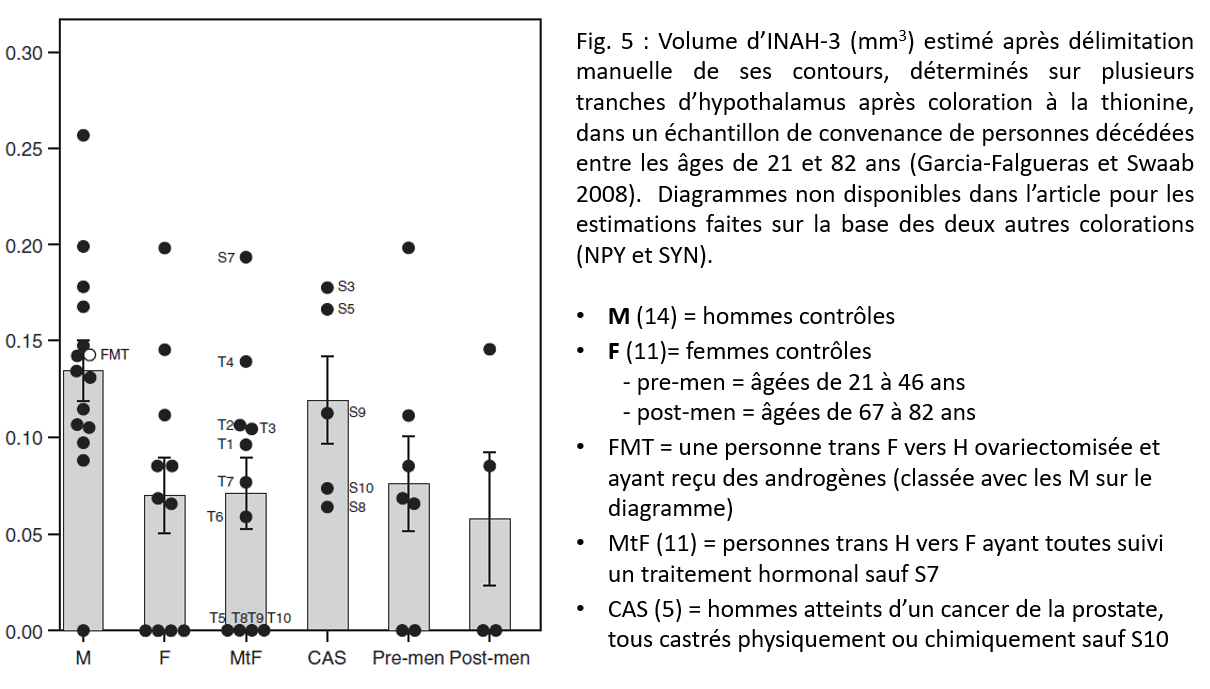
Bonjour,
Il est difficile pour moi d’y voir clair sur le sujet des différences biologiques entre les hommes et les femmes tant les avis (même des experts) semblent opposé. Ainsi, puisque vous semblez objective et non dans une démarche idéologique, j’aimerais vous poser la question suivante, qui est très simple : il y a-t-il des études scientifiques qui révèlent des différences de comportement biologiques entre les hommes et les femmes ? Ou alors les différences que nous observons sont-elles seulement culturelles ?
Vous avez déjà du répondre souvent à cette question mais étant novice, il est très difficile pour moi d’y trouver une réponse. Je serais preneur de références.
Merci.
Bonjour. En bref, la réponse que je fais à cette question se trouve par exemple dans https://allodoxia.odilefillod.fr/2013/10/04/sexes-mensonges-et-video-baron-cohen/#comment-1640. Vous trouverez des précisions (notamment concernant l’angle particulier sous lequel j’abord cette question en lien avec ses enjeux idéologiques, auxquels je ne prétends pas du tout être indifférente) dans la suite de l’échange sur ce commentaire, qui commence à https://allodoxia.odilefillod.fr/2013/10/04/sexes-mensonges-et-video-baron-cohen/#comment-1656), ainsi que dans cette autre réponse que j’ai faite dans https://allodoxia.odilefillod.fr/2012/03/12/maternite-science-feminisme/#comment-1176
Merci d’avoir pris le temps de me répondre.
Bonne journée.
Bonjour
Tout d’abord je veux vous dire merci pour ce travail très important et sourcé que vous effectuez.
Je ne remet pas en cause ce travail et n ai pas encore lu une grande partie de ce dernier (j ai commencé récemment).
Je me permet, malgré ma faible connaissance en la matière toute fois, quelques remarques ou questions..
Dans votre votre (très bonne) interview dans Meta de Choc, vous avancez que de nombreux médicaments ont été testés sur les souris et ne fonctionnent pas chez l’humain, il est vrai que de nombreux médicament n’ont pas d’effet avéré, (30 % d’après mes sources), mais il me parait “rapide” d’attribuer cela au support des essais, les souris, vous connaissez comme moi les nombreux autres biais dont le premier, l’intérêt économique des laboratoires et la faiblesse consécutive de bon nombre de leurs études.
A partir de ce constat et étant d’accord avec vous sur l’absence de preuve définitive apportée par les modèles d’expériences sur les animaux, ne peut on tout de même accepter une approche bayésienne, en l’absence d’autres théories plus valides, et présenter ces connaissances comme “plus probables actuellement”…(par ex les expériences de la transmission épigénétique du stress chez la souris, Isabelle Mansuy, Université de Zurich) ?
En effet nous sommes confrontés à des choix de société, comment éduquer, comment soigner, et devons baser nos actions sur des théories.
Le risque d’un relativisme excessif serait de laisser chacun imposer ses théories, ainsi ce relativisme fait le jeux des psychanalystes dont certains proposent encore des séances de thérapie de conversion pour les homosexuels par exemple, pour revenir sur votre sujet de prédilection.
Je reste bien sur ouvert à toute explication du choix de notre sexualité, qu’elle soit “naturelle” ou d’influence sociale, multiple même possiblement.
La “vérité” est rarement un phénomène simple un aborder et demande en effet beaucoup d’humilité.
Encore merci pour vos recherches et votre travail de vulgarisation, je vais continuer à lire votre blog.
Bien cordialement.
Merci pour vos retours sur le blog et sur l’interview.
Dans le passage de celle-ci auquel vous faites référence, la question qui m’est posée est : “si on observe des réactions à la testostérone, par exemple, chez la souris, pourquoi elles seraient pas applicables à l’humain ?”. Dans ce contexte, j’explique qu’on ne peut en général pas extrapoler automatiquement à une espèce X toute observation faite dans une espèce Y (dirait-on de même : “si une observation est faite chez l’être humain, pourquoi ne serait-elle pas applicable à la souris ?” ?), puis je donne un exemple concert appliqué au domaine dont nous parlons dans cette interview (la différence manifeste entre rongeurs et primates dans l’importance des effets de l’aromatisation locale de la testostérone durant le développement précoce du cerveau sur les comportements sexuels ultérieurs), et enfin je rappelle effectivement que les chercheur.es ne cessent de trouver des molécules “prometteuses” qui semblent bien marcher sur des souris, mais qui n’aboutissent pourtant jamais à un médicament développé (parce qu’il s’avère toxique ou inefficace chez l’être humain).
Les recherches sur les souris dont il est question ici relèvent de recherches faites très en amont. Entre ce genre de recherches et la mise sur le marché de médicaments destinés aux humains, des essais sont toujours faits sur des êtres humains. Absolument toujours, et ce précisément pour la raison que j’indique. Le pourcentage que vous donnez – que je crois être une estimation (discutable) du pourcentage des médicaments actuellement sur le marché et n’ayant pas un effet supérieur à un placebo, mais dites-moi si je me trompe – n’a rien à voir avec la problématique de l’extrapolation de la souris à l’humain.
Pour l’extrapolation de modèles animaux à l’humain en général, et pour le sujet sur lequel je suis interviewée en particulier (les différences psychologiques entre femmes et hommes qui seraient causées par des mécanismes de sexuation biologique du psychisme), on ne dispose pas des éléments qui seraient nécessaires à la mise en place d’une approche bayésienne.
Par ailleurs, en ce qui concerne ce sujet, je tiens à souligner qu’on ne peut pas parler d’absence d’autres théories plus plausibles. Au contraire, des hypothèses alternatives existent et reposent quant à elles sur des mécanismes dont les effets ont été concrètement observés chez l’être humain. Si on appliquait le principe du rasoir d’Ockham, ce sont à mon avis plutôt ces hypothèses-là qui devraient être privilégiées…
Pour ce qui est de l’orientation sexuelle, je précise d’abord que ce n’est pas mon “sujet de prédilection”. Le sujet sur lequel je travaille principalement, ce sont les explications biologiques des différences cognitives et comportementales entre femmes et hommes. C’est dans ce cadre que j’aborde la question de l’orientation sexuelle, car il s’agit de la plus nette (et de loin) des différences observées entre femmes et hommes, et qu’il est intéressant de se pencher sur la fausse évidence de son caractère naturel.
Quant aux “thérapies de conversion”, il n’est nul besoin d’adopter telle ou telle théorie sur les “causes de l’homosexualité” pour s’y opposer. Leur profonde contradiction avec l’éthique du soin, non seulement dans leur principe mais du fait des souffrances concrètes que cela inflige indûment aux personnes qui y sont soumises sous une pression sociale, y suffit.
Merci du temps pris pour me répondre.
Je suis désolé de m’attarder sur les points qui me chiffonnent, cela peut amener à penser que je contredis l’ensemble de vos affirmations, bien au contraire j’y adhère largement, mais c’et en s’attachant aux points de désaccords que nous progressons le plus, pas en se congratulant constamment.
Tout d’abord je ne suis pas centré sur le comportement sexuel mais plus sur l’impact de la métacognition sur nos comportements, cependant la lecture de vos écrits m’apporte beaucoup tout de même.
Concernant le pourcentage de médicaments n’ayant pas un effet supérieur au placebo, c’est un chiffre grossier en effet discutable, dépendant de la taille d’effet retenue et bien d’autres facteurs, issu de mes échanges avec mon frère médecin et ancien chercheur en biologie, donc pas d’une lecture directe pour moi, mais cela va dans votre sens, d’ou mon approximation.
Il n’y a pas de raison que l’extrapolation de mécanismes issus de la recherche sur les animaux, aux humains ne puisse faire l’objet d’approche bayésienne.
Toute question peut le faire, se voyant attribuer une probabilité allant de 10 puissance-x à 10 puissance x, x n’ayant pas de limite, cette probabilité excluant juste le 1 et le 0, donc toute certitude, (même pour la proposition ” la terre est plate”, x devenant extrêmement grand par ex).
Il est possible de partager le chiffre 1 en 2, 3 ou plus de manière équitable si aucune hypothèse n’est à privilégier, sans etre fort en probabilités, je ne vois pas de raison de ne pas appliquer l’approche bayésienne aux théories sur les comportements sexuels.
j’espère ne pas paraître trop docte dans mes explications, je suis conscient de votre maîtrise bien supérieure à la mienne des questions statistiques.
J’ai chercher sur votre site une critique de l’étude sur la reconnaissance faciale de l’orientation sexuelle, (Yilun Wang, Michal Kosinski, 2018, http://psycnet.apa.org/doiLanding?doi=10.1037%2Fpspa0000098) ( sans la trouver, je pense que je n ai pas identifié le bon emplacement, sachant que sa lecture partielle, (je ne possède pas l article entier montre déjà quelques biais dont le mélange de traits physiologiques et des ajouts (“style de toilettage”).
Pour autant la piste biologique de l’orientation sexuelle ne me semble pas devoir etre abandonnée, car je n’ai pas trouvé mieux coté social.
La piste Biologique serait déculpabilisant pour de nombreux parents, contrairement à de nombreuses thèses psychanalytiques par ex, même si bien sur nos désirs ne doivent pas orienter notre lecture.
De nombreuses études portes sur les mammifères et montrent de ressemblances physiologiques avec l’humain or il est difficile de réfuter l’importance du substrat physiologique sur nos comportements (maladies, troubles hormonaux, épigénétique visiblement etc), cela ne constitue en rien une preuve pour le cas de l’orientation sexuelle, bien entendu, mais quelle meilleur piste avons nous pour orienter les recherches ?
Je reste ouvert à toute hypothèse, n’étant d’ailleurs pas touché directement par cette question, bien que fréquentant régulièrement le milieu LGBT par ma famille et mes amis).
encore merci à vous…
cordialement
Ne soyez pas désolé de focaliser la discussion sur des points de désaccord, c’est au contraire ce qui m’intéresse le plus dans les échanges. Les félicitations ou remerciements ne font effectivement pas progresser la réflexion (cela dit, que les personnes qui ont envie de faire ce genre de commentaires ne se privent surtout pas, ça fait plaisir et ça m’encourage à poursuivre mon travail bénévole et souvent ingrat !). L’apport de nouveaux arguments allant dans le même sens que les miens m’intéresse aussi, mais moins que l’inverse.
Il y a beaucoup de sujets différents dans votre commentaire, et je n’ai pas le temps de répondre sur tous dans l’immédiat. Je réponds d’abord sur la question de l’approche bayésienne et traiterai la suite plus tard.
J’avais donc bien compris que les 30% que vous aviez indiqués ne concernaient pas l’extrapolation de la souris (par exemple) à l’humain. C’est là que réside il me semble un des problèmes avec l’idée d’appliquer une approche bayésienne.
En effet, mettons que vous vouliez estimer la probabilité que chez l’humain, tel facteur biologique est la cause d’au moins tel pourcentage de la variance dans telle mesure de l’orientation sexuelle, et appelons cette probabilité P(H). Dans le cadre de l’approche bayésienne classique de l’analyse de données expérimentales, vous allez définir une valeur a priori pour P(H), puis à chaque nouvelle observation pertinente que vous prendrez en compte (O), vous allez affiner votre estimation en calculant P(H/O) (= probabilité de H sachant O) comme suit : P(H/O) = P(O/H) * P(H) / P(O). Ce n’est déjà pas évident à mettre en oeuvre quand les observations dont on dispose ne sont pas parfaitement pertinentes par rapport à l’hypothèse formulée. Mais ce que vous proposez de faire me semble encore plus difficile. Car si je comprends bien, votre idée serait d’affiner l’estimation de P(H) en utilisant des observations faites non pas directement sur l’objet de l’hypothèse, mais sur des modèles animaux de la relation entre le facteur biologique et la mesure de l’orientation sexuelle. Comment allez-vous estimer (quantifier) la pertinence de l’approximation des mesures faites chez ces animaux, et en particulier comment prendrez-vous concrètement en compte le fait que les mesures de l’ “orientation sexuelle” utilisées chez eux peuvent d’une part donner des résultats assez différents selon la mesure et selon l’espèce, et d’autre part n’avoir pas grand chose à voir avec la notion d'”orientation sexuelle” telle que définie opérationnellement par la mesure humaine choisie ? Mobiliseriez-vous une estimation de la probabilité d’ “applicabilité” à l’humain de n’importe quoi observé dans telle ou telle espèce (ou plutôt lignée, car on l’ignore trop souvent, mais il arrive régulièrement que des résultats trouvés dans telle lignée de rat de laboratoire, par exemple, ne soient pas retrouvés dans une autre) ? Comment feriez-vous, très concrètement ?
Pour ce qui est de l’étude de Wang et Kosinski sur la “reconnaissance faciale de l’orientation sexuelle”, je m’y étais penchée car elle avait fait un gros buzz, mais je n’ai rien publié à ce sujet sur mon blog. De bonnes critiques en ont été faites ailleurs. Je vous recommande en particulier celle faite sur le fort pertinent site Calling Bullshit, du biologiste Carl Begstrom et du chercheur en “sciences de la science” Jevin West : https://callingbullshit.org/case_studies/case_study_ml_sexual_orientation_original_version.html
Je pense comme eux qu’une explication très plausible de la relativement bonne performance observée de la machine, c’est que la présentation de soi des personnes sur les photos postées par elles sur un site de rencontre (c’est cela qui a été utilisé dans l’étude) n’est pas indépendante de leur orientation sexuelle, et que ce que la machine a appris à reconnaître, ce sont ces marqueurs culturels adoptés par les personnes selon leur plus ou moins grande identification sociale à tel ou tel groupe d’orientation sexuelle et selon le type de personnes aux yeux desquelles elles veulent apparaître séduisantes. Ca peut relever du style (ex : style de rasage pour les hommes, maquillage ou non pour les femmes) ou de l’attitude (ex : le fait de plus ou moins sourire sur la photo, sachant que c’est un marqueur de genre important). Sur le sourire, j’ai d’ailleurs remarqué que le portait-type homo masculin souriait plus que l’hétéro, et inversement pour les femmes. Begstrom et West ne le relèvent pas ici, mais ils avaient mis le doigt sur ce point au sujet d’une autre étude du même type, digne comme elle de la physiognomonie du 19ème siècle :
https://callingbullshit.org/case_studies/case_study_criminal_machine_learning.html.
Pour le reste de votre commentaire :
– Personne ne nie l’importance du substrat physiologique de nos comportements, mais comme vous le soulignez à juste titre, cela ne constitue en rien une preuve de quoi que ce soit concernant les différences d’orientation sexuelle. Je me permets de vous renvoyer à cette conférence que j’ai donnée en mars dernier sur l’état des recherches de facteurs biologiques innés de l’orientation sexuelle chez l’être humain : https://www.youtube.com/watch?v=m-RDg3OHXrY.
– Je n’ai aucun doute quant au fait que la “piste biologique” n’a pas à être abandonnée, au sens où des facteurs biologiques innés ont sans aucun doute une influence sur l’orientation sexuelle, mais toute la question est de savoir lesquels et par quels chemins éventuellement très indirects ils opèrent (i.e. avec des médiations par l’environnement psycho-affectif, social et culturel).
– La “piste biologique” au sens de l’hypothèse d’une détermination à 100% par des facteurs biologiques innés serait certes déculpabilisante pour de nombreux parents, mais elle n’a strictement aucune chance d’être correcte ; on le sait déjà. Il me semble qu’il vaut mieux s’attaquer aux causes sociales de ce sentiment indu de culpabilité, indu non parce que l’environnement d’élevage des enfants n’aurait à coup sûr aucune influence sur l’orientation sexuelle, mais parce que personne ne devrait se désoler d’avoir un enfant homosexuel.
– Pour ce qui est des autres facteurs, et en particulier des facteurs sociaux, il n’y a heureusement pas que les théories psychanalytiques ! Pour une approche sociologique de la question, je vous recommande la lecture de Nouvel éloge de la diversité sexuelle, par Michel Dorais (2019, vlb éditeur). Voir aussi cet article pour une approche à la fois socio-historique et critique d’une certaine théorisation psychanalytique : https://blogepervier.wordpress.com/2017/12/02/homosexualite-quand-freud-fait-de-la-biologie/
– Quant à l’extrapolation des résultats de certaines études animales à l’être humain, elle est particulièrement délicate sur ce sujet. Et comme je l’ai déjà souligné ailleurs, je ne vois pas pourquoi on devrait faire le pari que le déterminisme biologique de l’orientation sexuelle dans notre espèce est plus proche de son équivalent chez le rat que de son équivalent chez le bonobo.
Bien bonjour Madame Fillod,
Avant tout, je tiens à vous dire à quel point cet article (ainsi que les autres de votre blog) en deux partie que j’ai finis de lire récemment est passionnant, généreux, rigoureux, très bien référencé et, enfin, agréable à lire. Et pourtant je vous assure que la littérature scientifique à plutôt tendance à me causer des maux de tête. Plus sérieusement, je me demande s’il est possible de ne pas être admiratif/admirative devant un tel travail de recherche et d’écriture ! J’aimerais savoir être aussi assidue que vous mais ce n’est pas pour moi je crois. Mais quel plaisir que ce soit le cas de certaines personnes, en l’occurence vous-même, qui y mettez au service du débunkage scientifique (au passage, désolée si le terme ne convient pas, je ne m’y connais pas et dis peut-être des mots incorrects bien malgré moi je vous l’assure), ce qui est très important.
Ensuite, je ne peux réfréner une question qui me taraude suite à ma lecture toute récente de ces deux parties de votre article : Ainsi, si j’ai bien compris, même si une androgénisation prénatale (dérèglement hormonal) avait lieu, modifiant ainsi la taille du noyau de cerveau, l’effet de cela sur l’orientation sexuelle, ou plutôt les comportements sexuels peut-être, serait trop modeste pour être à l’origine de ces comportements. Mais est-ce que le fait qu’il y est tout de même un effet (imaginons…), aussi modeste soit-il, ne validerait-il pas, au moins un peu, le sexisme, en tout cas pour une partie des individus ? C’est à dire, en gros, le fait que les hommes gays seraient féminisés et les femmes lesbiennes masculinisées. D’ailleurs, cela pourrait même permettre amplement de penser que, pour d’autres cas, il y a une ou plusieurs autres raisons tout aussi validatrices du sexisme.
Je croise en tout cas les doigts, dans l’attente de votre réponse, pour que ce ne soit pas le cas ! Et j’espère aussi ne pas avoir une question bête en plus d’empiéter sur votre temps qui est sans le moindre doute bel et bien précieux.
Merci pour vos compliments 🙂
Pour répondre à votre question, s’il s’avérait que :
– la taille du noyau INAH-3 dépend du niveau d’exposition prénatale aux androgènes,
– la taille de ce noyau a un effet sur le degré de gynophilie et/ou androphobie sexuelle ultérieur,
– cet effet suit une fonction monotone croissante, c’est-à-dire que plus ce niveau est élevé, plus la personne sera gynophile et/ou androphobe,
alors pour moi cela pourrait valider l’idée que sur un certain plan tout au moins, certains hommes gays au moins sont biologiquement féminisés et certaines femmes lesbiennes au moins sont biologiquement masculinisées, mais surtout cela validerait plus généralement l’idée qu’hommes et femmes ont en moyenne des psychismes naturellement différents du fait de leurs constitutions biologiques différentes. Mais si cela peut vous rassurer, ces trois “si” sont à ce jour bien loin d’être avérés.
Merci énormément pour votre réponse ! En tout cas, ces trois « si » serait catastrophique si c’était le cas, et ce à plusieurs niveau. Effectivement, c’est rassurant de savoir qu’on est loin d’avoir avéré cela. Et aussi, ce qui me rassure également, c’est qu’à priori on ne pourrait pas y tester, sous peine d’enfreindre des lois éthiques.
A mon avis, les progrès technologiques (dont de l’imagerie in vivo) permettront tôt ou tard de faire des études longitudinales sur des personnes dès le state fœtal et ainsi de trancher cette question. Je serais étonnée qu’elles soient interdites pour des raisons éthiques.
L’idée qu’il n’est pas impossible que le sexisme soit validé est terrifiant. Pensez-vous qu’il y a des raisons de s’inquiéter ?
Pour ma part ça ne m’inquiète pas, car au vu des données déjà disponibles il me paraît très improbable qu’on découvre un jour qu’il existe de tels mécanismes de sexuation naturelle du psychisme humain ayant des effets notables.
C’est à cela que je m’accroche et le fait que vous aussi trouviez cela improbable étant donné tout ce que l’on sait déjà sur le psychisme humain comme vous le dites très bien, me rassure. Vos travaux, exhaustifs et rigoureux, me font avoir confiance.
Je vous remercie encore et vous souhaite un agréable week-end.
Je commencerai par vous dire merci de rendre accessible votre travail, par ce blog et son espace commentaire passionnant.
Pourriez-vous m’éclairer très rapidement sur ceci :
– Soutenez vous qu’il n’y a pas de différences cérébrales (anatomiques, fonctionnelles) entre homme et femme ? ; ou pas de différences innées ? ; ou pas de différences innées supérieures à la simple différence interindividuelle ? ; ou simplement que les différences observées n’impliquent pas de différences psychiques ou comportementales (qui serait alors en partie “naturelles”) ?
– Que pensez-vous de cette étude sur les fœtus ? Wheelock M.D. et al. (2019) https://www.sciencedirect.com/science/article/pii/S1878929318301245
Je l’ai trouvé via cet article de Christophe Rodo (https://cervenargo.hypotheses.org/2829) avec qui j’ai eu un rapide échange dont voici la conclusion :
“Les différences cérébrales existantes entre homme et femme est un sujet extrêmement complexe et il est à étudier avec certaines précautions méthodologiques. Néanmoins, il semble apparaitre que conclure que le cerveau homme serait en tout point identique au cerveau femme serait de l’ordre du neuromythe, mais conclure qu’ils seraient en tout point différent, le serait tout autant. Ces différences semblent liées à une interaction complexe de facteurs génétiques et environnementaux. Toutefois, ces différences ne semblent observables que lorsque des groupes sont étudiés. Car, ces résultats sont bien le fruit de calcul de moyenne et non l’étude d’individus isolés et comparés.”
ps : J’avais lu l’entièreté de ce présent articule à l’époque (et ses commentaires), et je n’ai pas le temps de m’y replonger entièrement ; veuillez m’excuser pour la redondance éventuelle de ma question.
– Je ne soutiens aucune des options que vous proposez, et la notion de “différences innées supérieures à la simple différence interindividuelle” n’a pas de sens pour moi. Les études comparant un groupe d’hommes à un groupe de femmes sur le plan cérébral (anatomie ou fonctionnement) ou sur le plan psychologique (cognitif ou comportemental) et ayant une puissance statistique suffisante trouvent fréquemment des différences moyennes statistiquement significatives entre eux. Il existe au moins une différence cérébrale naturelle, i.e. qui découle de la différence de sexe biologique via des mécanismes biologiques indépendants des vécus, socialisation, alimentation, etc, différents entre F et H : le cerveau des H est en moyenne plus volumineux que celui des F. Il existe au moins une différence moyenne constatée systématiquement dans toutes les sociétés : les H sont beaucoup plus souvent que les F plus attirés sexuellement par les femmes que par les hommes et réciproquement. Par ailleurs, il existe des anomalies génétiques qui sont à l’origine de troubles neurodéveloppementaux et qui n’ont en moyenne pas les mêmes conséquences selon le sexe (nombre d’anomalies du chromosome X sont plus délétères chez les garçons car il n’en ont qu’un). Je soutiens qu’en dehors du cas particulier de ces troubles, la recherche scientifique n’a pas permis d’établir l’existence de différences cérébrales naturelles (au sens défini plus haut) se traduisant par des différences cognitives ou comportementales.
– Ce que vous a écrit Christophe Rodo est ridicule : “il semble apparaitre que conclure que le cerveau homme serait en tout point identique au cerveau femme serait de l’ordre du neuromythe, mais conclure qu’ils seraient en tout point différent, le serait tout autant”. Il faudrait qu’il commence par expliquer ce qu’il appelle “cerveau homme” et “cerveau femme”, et parler de cerveau “en tout point identique” ou “en tout point différent” n’a aucun sens.
– Pour ce qui est de Wheelock M.D. et al. (2019), voici quelques éléments.
Ce qui est comparé entre filles et garçons dans cette étude est la corrélation entre l’âge gestationnel et la connectivité apparente entre 16 “réseaux cérébraux fœtaux putatifs” contenant en tout 197 régions cérébrales (les ROI produits par un algorithme qui partitionne les cerveaux de manière automatique).
NB1 : L'”approche statistique innovante” utilisée ici, mise au point et utilisée pour la première fois en 2017 par les auteurs, est inspirée des études d’association pangénomiques. Dans ces dernières, elle permet de trouver une association entre le trait étudié et un ensemble de gènes lorsqu’on échoue à en mettre en évidence une entre le trait et un gène isolé. Comme il n’existe pas de regroupements de régions “canoniques” identifiés dans le cerveau fœtal, les auteurs ont utilisé leurs données pour fabriquer des regroupements ad hoc qu’ils ont qualifié de “réseaux cérébraux fœtaux putatifs”. Il aurait été plus propre d’utiliser un autre échantillon de données pour établir ces réseaux car cette façon de procéder augmente le risque de “voodoo correlations” (voir https://cogns.northwestern.edu/cbmg/Vul2009PsycholSci.pdf).
NB2 : Les comparaisons utilisant directement les 197 régions ne sont pas rapportées, seules celles utilisant ces regroupements l’étant. Il est permis de douter que seules ces comparaisons ont été faites et pas aussi des comparaisons au niveau plus fin (les régions prises deux à deux), puisqu’une matrice de corrélations 197 x 197 a été produite par les auteurs, ainsi que des comparaisons de la connectivité elle-même plutôt que de son évolution avec l’âge gestationnel : il faisait sens de comparer entre groupes de sexe ces résultats, bien plus immédiats. Il est par conséquent permis de douter que la correction pour comparaisons multiples faite par les auteurs pour évaluer la significativité statistique des différences finalement trouvées grâce à leur approche statistique alambiquée est suffisante.
La connectivité apparente est elle-même déduite de la force de la corrélation entre l’intensité de l’activation de ces régions, cette activation ayant été mesurée au moyen d’une IRM fonctionnelle. Pour cela, un échantillon de 118 foetus a été utilisé (70 garçons et 48 filles) et parmi eux, seuls 21 ont eu leur cerveau scanné deux fois au cour de la gestation, une fois entre 26 et 28 semaines et une autre entre 35 et 37 semaines. C’est un très petit échantillon de données pour étudier la différence entre les sexes d’une évolution au cours de la gestation… Par ailleurs, les auteurs disent avoir contrôlé le parasitage induit par le mouvement des fœtus mais on se demande comme cela a pu être fait proprement quand on sait que le mouvement pose déjà des problèmes quand on scanne des gens immobilisés dans un appareil à IRM. De plus, ils n’ont pas appliqué de méthode appropriée de contrôle par le volume du cerveau, ce qui est aussi un souci pour interpréter leurs observations.
– Sur les 136 comparaisons filles-garçons rapportées (= 16 x 15 / 2 comparaisons de corrélation entre âge et connectivité entre deux “réseaux putatifs” + 16 comparaisons de corrélation entre âge et connectivité entre deux régions d’un même “réseau putatif”), seules 6 ont donné une différence statistiquement significative entre filles et garçons, et parmi celles-ci seules 3 étaient cohérentes avec l’évolution intra-groupe de sexe (i.e. la connectivité augmentait en moyenne significativement avec l’âge dans le groupe de sexe présentant en moyenne une plus grande augmentation de connectivité avec l’âge que l’autre groupe). Il s’agit des deux carrés rouges et du carré bleu de la fig.3 (https://ars.els-cdn.com/content/image/1-s2.0-S1878929318301245-gr3_lrg.jpg) : l’augmentation de la connectivité avec l’âge gestationnel a été en moyenne plus grande chez les filles que chez les garçons pour les paires Cervelet-Gyrus frontal supérieur gauche et Cortex cingulé postérieur-Pole temporal gauche (carrés rouges) et elle a été en moyenne plus grande chez les garçons que chez les filles pour la paire Cervelet-Cervelet (carré bleu).
NB3 : les carrés plus clairs sont commentés dans l’article en termes de différences entre le sexes mais il s’agit d’une interprétation incorrecte car ils ne correspondent pas à des différences statistiquement significatives entre eux.
NB4 : on n’a strictement aucune idée de ce que peuvent signifier ces (quelques) différences moyennes trouvées dans cet échantillon.
En bref, cette étude préliminaire faite sur un petit échantillon n’établit rien en l’attente de réplication ou au moins de la publication de résultats concordants. Elle comporte un haut risque de ne mettre en avant que des faux positifs et ses résultats ne peuvent être interprétés en termes de différences futures de fonctionnement des cerveaux des enfants concernés. C’est un comportement typique chez certains vulgarisateurs de se jeter sur ce genre d’études (dont les auteurs annoncent fièrement qu’elle “demonstrates for the first time that development of fetal brain FC [functional connectivity] varies with sex”) dès qu’elles sortent pour alimenter leur blabla.
Voilà une réponse parfaitement claire et qui m’était absolument nécessaire pour ne pas répandre des idées trompeuses autour de moi. Étant un passionné de science (et de pensée critique) sans expertise sur ce sujet précis, vous comprendrez qu’il n’est pas toujours facile de nuancer les informations qui s’accumulent de sources diverses. (Et c’est aussi pourquoi votre travail est si important.)
Je note donc les quelques pistes de critiques attribuables à cette étude, sans être en mesure de m’y attarder.
(Je précise que les mots employés par Chritophe Rodo (qui m’a très gentiment répondu) résultaient en partie de ma question, et qu’il n’y a sans doute pas mis la rigueur attendue pour une discussion plus importante.)
Merci.
Dans un livre de Pascal Pick (Premiers hommes) on peut lire dans un chapitre sur les singes que chez les enfants chimpanzés, les garçons préfèrent les jeux de bâtons et les petite bagarres tandis que les filles jouent a la poupée avec les petites sœurs. Tiens donc, nos plus proches cousins se comportent comme nous. incroyable, la construction sociale du genre existe aussi chez les chimpanzés ^^
Connaissant le tropisme / les croyances de Pascal Picq (avec un q) concernant les différences femmes-hommes et son manque de rigueur, je ne serais pas étonnée qu’après tant d’autres dont je n’ai donné qu’un petit échantillon, il fasse dire n’importe quoi à certaines études sur certains singes : https://allodoxia.odilefillod.fr/2014/07/23/camion-poupee-jeux-singes/. J’ose espérer qu’il ne va quand même pas jusqu’à exprimer les choses de manière aussi caricaturalement fausse et ridiculement anthropomorphique que vous. Si d’aventure vous avez trouvé dans son livre des éléments solides susceptibles de remettre en question ce que j’ai écrit dans l’article donné en lien ci-dessus, n’hésitez pas à le signaler en commentaire sous ce dernier plutôt qu’ici, ces considérations n’ayant qu’un rapport lointain avec le sujet du présent billet.
PS : sur les jeux de certains chimpanzés communs avec des bâtons, qui ne sont pas l’objet de mon billet de 2014, j’attire votre attention sur le passage suivant de celui-ci : “Dans la suite de l’article, elle reformule et réinterprète allègrement une observation faite sur la façon dont les jeunes chimpanzés d’un parc national ougandais utilisent les bâtons qu’ils trouvent dans la nature. Je ne m’étendrai pas sur cette manipulation qui mériterait un long développement, me contentant de souligner deux différences entre les propos des chercheurs et les siens. D’une part, alors que la journaliste prétend que ces résultats « montrent clairement que si les jeunes primates jouent tous avec des bâtons, les femelles aiment les porter, les bercer, comme des poupées, de manière maternelle sans équivoque », les auteurs de l’article scientifique écrivent quant à eux que « les jeunes tendent à porter les bâtons d’une manière évoquant un jeu à la poupée rudimentaire », et que « ce comportement est plus fréquent chez les femelles que les mâles ». D’autre part, alors que le titre à la Une du Figaro extrapole cette observation aux chimpanzés en général et que Martine Perez la présente comme un indice de l’existence d’une sexuation biologique non seulement des comportements des singes en question, mais des choix de jouets humains, l’auteur correspondant de l’article soulignait ceci dans le communiqué de presse annonçant sa publication : « Chez les êtres humains il existe à l’évidence un rôle énorme de l’influence des pairs, des parents et autres sur les préférences d’un enfant pour différentes sortes de jouets, et il pourrait bien en être de même chez les chimpanzés. […] L’une des choses qui rend notre observation fascinante est qu’il n’existe guère d’indices de quoi que ce soit de comparable dans d’autres communautés de chimpanzés, ce qui soulève la possibilité que ces chimpanzés copient une tradition comportementale locale »”
Et sinon, puisque vous vous intéressez à ce que font nos plus proches cousins pour en tirer des conclusions sur les prédispositions naturelles au sein de l’espèce humaine, je vous invite à vous renseigner sur le bonobo, qui est notre tout aussi proche cousin que le chimpanzé commun.
Bonjour, rien à voir avec l’article à part le procédé, mais je suis écœuré par cet article qui il me semble n’est pas le premier du genre. Une “anomalie” physique serait le signe d’une anomalie mentale. Ca me parait d’une absurdité totale et très dangereuse pour les gens porteur de cette soit disant anomalie :
https://www.maxisciences.com/sante/psycho/les-psychopathes-auraient-plus-de-chances-davoir-cette-particularite-physique-selon-une-etude_art49861.html
C’est juste un énième article (des centaines ont été publiés) rapportant l’étude de corrélations entre des traits physiques ou psychologiques et le ratio 2D:4D, c’est-à-dire la longueur de l’index divisée par la longueur de l’annulaire. Les hypothèses sous-jacentes à ces recherches sont en gros que toute différence moyenne de 2D:4D observable entre deux groupes de personnes indiquerait une différence entre ces deux groupes dans le degré d’androgénisation prénatale ET que toute différence moyenne entre ces groupes pour le trait étudié serait causée par cette différence moyenne d’androgénisation prénatale.
Rem : j’ai publié en 2018 un petit billet critique sur l’usage du 2D:4D comme indice d’androgénisation prénatale, suite à des accusations d’ignorance et de “chauvinisme anti-darwinien” faites à mon endroit par Peggy Sastre et Robert Trivers. Voir https://allodoxia.odilefillod.fr/2018/02/17/un-indice-fiable-de-quoi/.
Dans l’article du Journal of Psychiatric Research dont Maxiscience fait un compte rendu racoleur et plus que trompeur, les auteurs rapportent avoir trouvé les ratios 2D:4D (de la main droite) MOYENS suivants sur leur échantillon de 80 adultes :
– 0.959 chez les 34 hommes avec trouble de la personnalité antisociale et/ou avec usage abusif d’amphétamines,
– 0.982 chez les 10 femmes avec trouble de la personnalité antisociale et/ou avec usage abusif d’amphétamines,
– 0.996 chez les 27 hommes “sains”,
– 1.000 chez les 9 femmes “saines”,
avec une variabilité importante au sein de chacun des 4 groupes.
Rem : dans une étude faite sur un échantillon de 324 adultes dont je rappelle les résultats dans le billet cité ci-dessus, les ratios moyens trouvés avaient été de 0.997 pour les femmes, soit la valeur moyenne trouvée ici chez les “hommes sains”, et 0.992 pour les hommes (et cette différence n’était pas statistiquement significative du fait de la grande variabilité de ce ratio indépendante du sexe, le 2D/4D variant sur cet échantillon de 0.881 à 1.103).
Bref, cet article ne parle pas d’une “anomalie” physique et la valeur du ratio 2D:4D d’une personne ne peut en aucun cas être interprétée comme étant le signe d’une anomalie mentale. Même dans l’hypothèse hautement improbable où on retrouverait ces différences de moyennes de manière générale, et non pas juste par hasard dans ce petit échantillon, cela ne permettrait en aucun cas de dire si une personne a un trouble de la personnalité antisociale et/ou fait un usage abusif d’amphétamines sur la base de la mesure du ratio 2D:4D de sa main droite.
PS1 : dans cette étude les auteurs ont aussi cherché à voir si le ratio 2D:4D était statistiquement associé à deux traits de la personnalité, à savoir l’intolérance à l’incertitude et le narcissisme vulnérable, et ils n’ont pas trouvé de corrélation statistiquement significative dans leur échantillon.
PS2 : dans la discussion de leurs résultats, les auteurs écrivent “Overall, both the present data and the overview on the state-of-the-art (see Introduction) suggest that the associations between 2D:4D-ratios and dimensions of psychological functioning does not appear to be uniform”, et c’est le moins qu’on puisse dire.
Merci beaucoup pour votre réponse